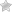Содержание
Отслойка сетчатки — это процесс отделения сетчатой оболочки глаза от сосудистой оболочки. В здоровом глазу они тесно соприкасаются. Отслойка сетчатки нередко приводит к значительному снижению зрения и слепоте. Чаще всего она возникает при травмах и близорукости, а также при диабетической ретинопатии, внутриглазных опухолях, дистрофиях сетчатой оболочки и т.д.
Нередко наш глаз сравнивают с фотоаппаратом, в котором роль объектива выполняет роговица и хрусталик: они пропускают и преломляют лучи света, попадающие в глаз. Роль светочувствительной пленки отведена сетчатой оболочке: на ней отображается все то, что мы видим. Сетчатка глаза состоит из множества нервных клеток и их отростков. Клетки, воспринимающие свет, называются колбочками и палочками. В сетчатке глаза человека палочек во много раз больше, чем колбочек: палочек — около 170 миллионов, колбочек — 8 миллионов. Под действием света в этих клетках зрительный пигмент распадается и образуются особые вещества-раздражители. Они вызывают своего рода электрический разряд, который, как по электрическим проводам, передается по нервным клеткам сетчатки, а затем по зрительному нерву в мозг. В коре головного мозга, а точнее, в его затылочной части, этот электрический сигнал превращается в зрительный образ.
Палочки и колбочки распределены в сетчатке неравномерно. У каждого вида этих нервных клеток свои особые функции. Колбочки сконцентрированы в центре сетчатки, в том месте, куда попадают лучи от рассматриваемых нами предметов. Они обеспечивают человеку высокую остроту зрения, восприятие всех цветов и их оттенков. Палочки обеспечивают нам сумеречное и боковое зрение, то есть позволяют видеть в сумерках и ориентироваться в пространстве. Палочки расположены сравнительно равномерно на всем протяжении сетчатки, но их количество увеличивается по мере удаления от центра.
В норме сетчатка тесно прилегает к сосудистой оболочке, от которой она получает питание.
Причины отслойки сетчатки
Основной причиной отслойки сетчатки является изменение стекловидного тела, приводящее к разрыву. Сетчатка не сдвигается со своего места, если она герметична (сохраняет свою целостность) и в ней нет разрыва. Если разрыв образовался, то через него жидкость из стекловидного тела проникает под сетчатку и отслаивает ее от сосудистой оболочки.
Основная причина формирования разрыва сетчатки — натяжение стекловидного тела при изменении его нормального состояния. Этот процесс происходит таким образом: в норме стекловидное тело напоминает прозрачное желе. В некоторых случаях оно изменяется, становится мутным с плотными тяжами, т.е. уплотненными волокнами, которые связаны с сетчаткой. При движении глаза тяжи тянут сетчатку за собой, что может привести к ее разрыву.
Разрывы сетчатки могут возникать также при ее дистрофии (истончении). Большие разрывы часто возникают при травмах глаза.
Симптомы отслойки сетчатки
Успех лечения отслойки сетчатки напрямую зависит от своевременного обращения к врачу. Чем раньше будет обнаружена болезнь и найдены ее причины, тем быстрее можно провести необходимое лечение и тем лучше окажется результат.
Что может указывать на начавшуюся отслойку сетчатки?
- появление «пелены» перед глазом. Пациенты безуспешно пытаются самостоятельно устранить ее, промывая глаза чаем или закапывая капли. В этом случае важно запомнить и сказать врачу, с какой стороны первоначально появилась «пелена», так как со временем она может увеличиться и занять все поле зрения;
- вспышки в виде искр и молний — также являются характерной чертой происходящего отслоения сетчатки;
- искажение рассматриваемых букв, предметов, выпадение из поля зрения их отдельных участков указывает на то, что отслоение захватило центр сетчатки.
Иногда пациенты отмечают, что после сна зрение несколько улучшается. Это объясняется тем, что при горизонтальном положении тела сетчатка возвращается на свое место, а когда человек принимает вертикальное положение, она вновь отходит от сосудистой оболочки и дефекты зрения возобновляются.
Отслойку сетчатки невозможно вылечить никакими каплями, таблетками или уколами. Единственный способ восстановить зрение и сохранить глаз — срочное проведение операции.
При отслойке сетчатки погибают нервные клетки, палочки и колбочки, и чем дольше существует отслойка, тем больше погибает этих клеток и тем хуже восстановление зрения даже после успешной операции.
ПОМНИТЕ! Если запустить болезнь, может возникнуть опасность хронического воспаления, развития катаракты, глаз может полностью потерять способность видеть. Особенно бдительными нужно быть тем людям, у которых уже была отслойка сетчатки на одном глазу. Им следует периодически обследоваться у офтальмолога. А при появлении подозрительных симптомов немедленно обратиться к своему врачу.
ДИАГНОСТИКА
Только специалист может определить, есть ли у Вас отслойка сетчатки, каков ее уровень, проведет Вам все необходимые обследования с помощью современного высокоточного оборудования.
Диагностика отслойки сетчатки требует следующих исследований:
- проверка остроты зрения, которая покажет состояние центральной области сетчатки;
- исследование бокового зрения (периметрия) для оценки состояния сетчатки на ее периферии;
- измерение внутриглазного давления (тонометрия). При отслойке сетчатки оно может быть ниже нормы (норма — 16-25 мм ртутного столба);
- специальное электрофизиологическое исследование позволит определить жизнеспособность нервных клеток сетчатки и зрительного нерва;
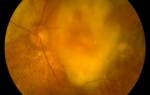
- осмотр глазного дна (офтальмоскопия). Это поможет точно определить места разрывов сетчатки и их количество, выявить истонченные участки, которые могут привести к возникновению новых очагов болезни;
- исследование с помощью ультразвука даст представление о размерах отслоившейся сетчатки и состоянии стекловидного тела. Это исследование особенно важно при помутнениях роговицы, хрусталика или стекловидного тела, когда увидеть сетчатку невозможно.
Энциклопедия пациента
| а | б | в | г | д | е | ж | з | и | к | л | м | н | о | п | р | с | т | у | ф | х | ц | ч | ш | э | ю | я |
открыть все
16 декабря 2020
По статистике, около 30% пациентов, переболевших COVID-19, жаловались на дискомфорт в глазах и различные расстройства зрения. В большинстве случаев эта проблема сохранялась на протяжении до 2 недель.
Конъюнктивит при коронавирусной инфекции развивается за счет проникновения вирусных частиц через слизистые оболочки глаз, которые являются «входными воротами» для вируса. Поэтому в общих рекомендациях по профилактике распространения COVID-19 сказано: нельзя прикасаться грязными руками к лицу, а также тереть глаза. Лучшим средством защиты глаз при данной инфекции являются очки, которые будут плотно прилегать к лицу, а также тщательная гигиена рук.
Часто признаки вирусного конъюнктивита появляются за несколько дней до острой иммунной реакции организма в виде повышения температуры тела. Уже после этого возникает общая слабость, боли в мышцах, нарушение обоняния.
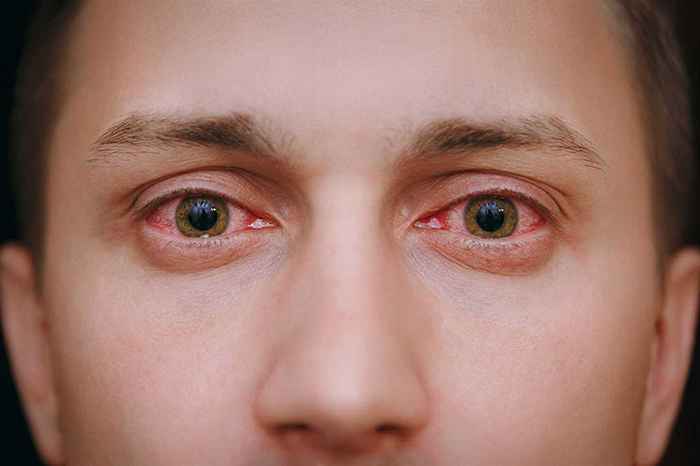
Общая клиническая картина поражения глаз включает в себя: покраснение глаз, светобоязнь, слезотечение, рези в глазах, ощущение сухости, чувство соринки, зуд, жжение, затуманенность, снижение остроты зрения. Чаще всего коронавирусная инфекция поражает оба глаза и клиническая картина в обоих глазах развивается одинаково.
Также учеными доказано, что коронавирусная инфекция живет на веках и ресницах до 2 суток. Интересен тот факт, что пациенты, жалующиеся на рези , покраснения и дискомфорт в глазах в комплексе с потерей обоняния, реже имели тяжелые формы COVID-19, в отличии от тех пациентов, у которых этих признаков не было. Болезнь у них протекала легче, без осложнений в виде пневмоний и сердечной недостаточности.
В группу риска попадают маленькие дети и пожилые люди, которые не всегда ответственно соблюдают правила личной гигиены. Увлекшись интересной игрой, дети часто прикасаются к лицу, трут глаза. Также высока вероятность заболеть тем, кто по роду своей деятельности вынужден контактировать с большим количеством людей. При сильном кашле, чихании возрастает вероятность распространения инфицированной слюны на несколько метров.
Слизистая оболочка глаза страдает от проникновения в нее коронавирусной инфекции — в ней развивается мощный воспалительный процесс, который может затронуть роговицу и сетчатку глаза.
Одним из способов профилактики проникновения в глаза коронавирусной инфекции является промывание слизистой глаз изотоническим раствором хлорида натрия (капли «Окусалин»). При первых признаках явного воспаления глаз следует незамедлительно обратиться к офтальмологу.
Соблюдайте правила личной гигиены, берегите себя и будьте здоровы!
вернуться к списку –> –> вернуться к списку Важное о COVID-19 Клиника Вся Медицина Все публикации
Ученые МФТИ в сотрудничестве с исследователями Гарварда вырастили клетки сетчатки, которые способны врастать в глаза. Это первая в мире успешная попытка трансплантации ганглионарных клеток (нейроны сетчатки, которые разрушаются при глаукоме), полученных из стволовых клеток в лабораторных условиях. Далее выращенные клетки нужно будет трансплантировать в сетчатку. Ученые проверили технологию на мышах и удостоверились в успешном встраивании клеток и их выживании на протяжении года. В дальнейшем исследователи планируют создать специализированные банки клеток, которые позволят индивидуально подбирать терапию для каждого пациента.
Операция «Трансплантация»
Первую в мире успешную попытку выращивания и трансплантации ганглионарных клеток сетчатки из стволовых произвели ученые лаборатории геномной инженерии МФТИ в сотрудничестве с исследователями Гарвардской медицинской школы. Ганглионарные клетки ответственны за передачу зрительной информации, и именно они повреждаются при глаукоме. Ученым удалось не только вырастить нейроны (ганглионары считаются специализированными нейронами), но и трансплантировать их в глаза мышей, добившись правильного врастания искусственной ткани сетчатки. Как известно, без лечения развитие глаукомы может привести к необратимому повреждению части зрительного нерва и, как следствие, потери части визуального поля. Прогрессируя в течение долгого времени, эта болезнь может привести и к полной слепоте.
В поле зрения: ученые открыли ген наследственной слепоты Болезнь вызывает мутация, из-за которой перестает вырабатываться важный белок
Клетки сетчатки были выращены в специальных органоидах, ткань формировалась в пробирке, рассказал «Известиям» младший научный сотрудник лаборатории геномной инженерии МФТИ Евгений Кегелес. Потом эти клетки пересадили мышам, которые были распределены в несколько групп.
— Были мыши с моделью глаукомы, мыши с повышенным внутриглазным давлением и те, у которых были удалены собственные ганглионары, — отметил Евгений Кегелес. — Были также новорожденные мыши: мы проверяли гипотезу более успешной приживаемости молодых ганглионарных клеток в формирующейся сетчатке. В результате оказалось, что клетки встроились и прорастили аксоны, которые позволят связать глаз с мозгом. Улучшенная выживаемость клеток у новорожденных мышей дает нам перспективное направление для поиска наилучшего микроокружения.
По словам Евгения Кегелеса, эти клетки успешно просуществовали внутри сетчатки 12 месяцев, что является серьезным сроком для такого исследования. Ученым удалось убедиться, что они получают зрительные сигналы, однако то, что клетки передают сигналы в мозг, со стопроцентной уверенностью утверждать пока нельзя.
— Мы точно знаем, что выращенные клетки встраиваются куда надо, протягивают аксоны в мозг, но их функциональность оценить пока невозможно, — объяснил Евгений Кегелес. — Это связано с тем, что до сих пор нам не удалось вырастить большое количество клеток. Это вопрос ближайших лет.
По его словам, исследователям нужен год, чтобы они смогли оценить функциональность клеток на мышиных моделях. В течение этого времени можно будет получить доказательство, что клетки не просто правильно встроены в структуру глаза, а они именно «видят».
Клеточный банк
Сейчас мышиные клетки сетчатки удается вырастить примерно за 21 день. В случае человека это будет от 50 до 100 дней, говорят ученые МФТИ.
Однако, скорее всего, человеку с глаукомой, готовящемуся к трансплантации, не нужно будет выращивать ткань сетчатки из собственных стволовых клеток. Так как глаз является иммунопривилегированным органом, где отторжения редки, возможно создать банк клеток для таких пациентов. Там будут размещены или выращенные клетки сетчатки от универсального донора, или из индуцированных плюрипотентных стволовых клеток. Это значит, что можно будет заранее вырастить клетки, заморозить их и, когда пациент с глаукомой обратится за помощью, подобрать для него наилучший клеточный вариант для трансплантации.
Земля не плоская: вернуть объемное зрение помогут компьютерные очки Разработанный российскими учеными прибор исправит серьезную патологию за несколько месяцев в домашних условиях
Впоследствии эту технологию можно будет применять и для лечения других заболеваний глаз, например дистрофии сетчатки. Однако выращивать придется другие клетки.
— Нобелевскую премию за индуцированные плюрипотентные стволовые клетки дали почти 10 лет назад, в 2012 году, — отметил руководитель лаборатории геномной инженерии Павел Волчков. — Так называемый хайп, когда буквально все научные коллективы считали своим долгом заниматься этой тематикой, давно угас. Сейчас настало время не просто слов, а реальных технологий на основе iPS (искусственные плюрипотентные стволовые клетки человека. — «Известия»). И именно к таким технологиям относится исследование по трансплантации ганглионаров сетчатки. Это возможность показать, что стволовые клетки реально можно применить на практике, с их помощью можно что-то исправить. Хотя эта работа еще не доведена до клиники, но она уже в нескольких шагах от реальной пересадки с целью лечения глаукомы.
Учитывая большой опыт экспериментальных работ мировых ученых и активное изучение вопроса заместительной клеточной терапии в офтальмологии, в дальнейшем метод может привести к прорыву в диагностике и лечении глаукомы, считает заведующая отделением офтальмологии ФГБУ НМИЦО ФМБА России, действительный член Европейского общества катарактальных и рефракционных хирургов (ESCRS), член Российского общества офтальмологов Ника Тахчиди.
Слепой метод: что помогает незрячим ориентироваться в телефоне и мире Прототипов сотни, реально доступных устройств — единицы
— В ряде зарубежных работ показано, что введенные клетки встраиваются в сетчатку и частично дифференцируются в клетки сетчатки. В настоящее время описаны и обсуждаются два основных механизма действия клеток in vivo и in vitro. Замещающая терапия — когда клетки, образующиеся в результате дифференцировки введенных стволовых клеток, «включаются» в восстанавливаемую ткань. «Эффект стороннего наблюдателя» — когда вводимые стволовые клетки оказывают противовоспалительное, трофическое или иммуномодулирующее действие на восстанавливаемую ткань. Однако, несмотря на прорыв в изучении морфофунциональных свойств стволовых клеток, обеспечить гарантированное послойное замещение культивированными клетками поврежденных участков сетчатки при использовании практикуемых методов введения на сегодняшний день невозможно, что и подтверждается рядом экспериментальных работ, — сказала Ника Тахчиди.
Впрочем, многие ученые в мире сейчас работают в этом направлении, пытаясь создать клеточную терапию лечения атрофии зрительного нерва, дистрофии сетчатки и глаукомы, отметила заведующая отделением офтальмологии клинико-диагностического центра «Медси», врач-офтальмолог Ирина Евсегнеева.
— Но никаких данных на сегодняшний день о том, что пересаженные клетки передают изображение, нет. Любая идея, как это сделать, заслуживает внимания, — сказала она.
По оценке ученых МФТИ, на доведение технологии до применения в лечебной практике уйдет примерно 10 лет.
Читайте также –>–>
Луцентис (ранибизумаб) представляет собой лекарственный препарат, основное назначение которого является интравитреальное введение с антивазопролиферативной целью. Интравитреальная инъекция является одним из самых эффективных методов терапевтического воздействия в современной офтальмологической практике. Таким способом лекарственные препараты могут попадать непосредственно к цели своего влияния – сетчатке глаза для лечении различной тяжелой патологии глазного дна. Сертифицированным лекарственным средством для интравитреального введения является препарат Луцентис, о котором и пойдет речь в данной статье.
Что такое Луцентис
Действующим веществом препарата Луцентис является ранибизумаб, который, с биохимической точки зрения, представляет собой фрагмент человеческого рекомбинантного моноклонального антитела, предназначенный для внутриглазного введения. Многие патологические состояния глазного дна, в том числе влажная форма макулярной дегенерации и диабетическая ретинопатия, сопровождаются разрастанием аномальных по строению и функциональным свойствам новообразованных кровеносных сосудов. Такие сосуды являются неполноценными, склонны к частым разрывам, что сопровождается кровоизлияниями в сетчатку глаза, стекловидное тело и субретинальное пространство.
Подобный патологический процесс является, по сути, бесконечным и приводит к необратимой потере зрения. Приостановить пролиферацию патологических кровеносных сосудов помогает особая группа препаратов – антивазопролиферативные агенты. К этой группе и относится ранибизумаб или Луцентис. Укол Луцентиса связывает и, тем самым, блокирует биологическую активность человеческого сосудистого эндотелиального фактора роста (VEGF), что и препятствует росту кровеносных сосудов.
Состав и форма выпуска Луцентиса
Препарат Луцентис представляет собой стерильный бесцветный или бледно-желтый слегка опалесцирующий раствор, находящийся в заполненном производителем одноразовом шприце или стеклянном одноразовом флаконе. Стерильный раствор содержит 10 мг/мл ранибизумаба. Вспомогательные вещества, содержащиеся в растворе, – гистидин, полисорбат, трегалозы дигидрат. Объем раствора во флаконе – 2,3 мл. Флакон препарата не может быть использован для нескольких пациентов, соответственно один укол Луцентиса рассчитан только на одно интравитреальное введение. Производитель препарата Луцентис – Novartis Pharma (Швейцария). Хранить препарат необходимо в холодильнике соблюдая температурный режим – 2-8 °C. Замораживать препарат запрещено. Хранить необходимо в защищенном от света месте. Нарушение условий хранения или транспортировки может повлиять на лечебные свойства препарата.
Механизм действия Луцентиса
Препарат Луцентис (Ранибизумаб) представляет собой фрагмент антитела к эндотелиальному фактору роста сосудов А (VEGF-A). Доказано, что именно VEGF-A вызывает неоваскуляризацию и пропотевание жидкости через сосудистую стенку, — процессы, лежащие в основе прогрессирования влажной формы макулярной дегенерации и других заболеваний сетчатки глаза. Применение Луцентиса приводит к связыванию VEGF-A, препятствуя тем самым взаимодействию молекул данного вещества с одноименными рецепторами (VEGFR1 и VEGFR2). Описываемые рецепторы локализуются на поверхности эндотелиальных клеток, выстилающих внутреннюю стенку капилляров. Укол Луцентиса приводит к редукции эндотелиальной пролиферации, уменьшению пропотевания жидкости через сосудистую стенку и формированию гораздо меньшего количества новых функционально неполноценных кровеносных сосудов.
По данным фармакокинетического анализа, период полувыведения ранибизумаба из стекловидного тела после укола Луцентиса при использовании стандартной дозировки 0, 5 мг составляет около 9 дней. Концентрация лекарственного препарата в плазме уменьшается пропорционально его элиминации из полости глазного яблока. Следует отметить, что концентрация ранибизумаба в плазме в 90000 раз меньше его концентрации в полости глазного яблока. Это означает, что системного действия препарат фактически не оказывает.
Показания к применению Луцентиса
Инструкцией по применению Луцентиса, а также данными множества научных исследований, определены следующие показания к интравитреальному введению данного препарата:
- Неоваскулярная (влажная) форма макулярной дегенерации.
- Отек макулы, возникающий в результате окклюзии ретинальной вены.
- Диабетическая ретинопатия, проявляющая отеком макулы.
- Хориоидальная неоваскуляризация, вызванная миопией.
Данный список показаний является общим. Необходимость интравитреального введения Луцентиса определяется лечащим врачом для каждого конкретного пациента исходя из клинической картины, а также динамики состояния глазного дна.
Частота приема и дозировка Луцентиса
Препарат Луцентис предназначен исключительно для интравитреального введения. Частота введения и режим дозирования зависит от вида патологии глазного дна:
- При неоваскулярной (влажной) форме макулярной дегенерации 0,5 мг (0,05 мл 10 мг/мл раствора) укол Луцентиса рекомендовано выполнять с интервалом 1 интравитреальное введение препарата 1 раз в месяц (минимальный промежуток между инъекциями – 28 дней). Во время лечения необходим периодический осмотр глазного дна и контроль остроты зрения. Допустимо урежение введения препарата после 3-хкратного последовательного введения при условии стабилизации состояния и улучшения остроты зрения. Допустимо, чтобы укол Луцентиса выполнялся 1 раз в 3 месяца после последовательного 4-хкратного применения препарата.
- Базовый режим дозирования при возникающем в результате блокады ретинальной вены отеке макулы, а также при диабетической патологии сетчатки аналогичный — 0,5 мг (0,05 мл 10 мг/мл раствора) Луцентиса рекомендовано для интравитреального введения 1 раз в месяц. Ежемесячный укол Луцентиса должен чередоваться с контролем состояния глазного дна и остроты зрения.
- Вызванная миопией хориоидальная неоваскуляризация требует интравитреального введения 0,5 мг Луцентиса каждый месяц в течение трех месяцев. По показаниям курс лечения можно повторять.
Контроль динамики заболевания осуществляется посредством оценки остроты зрения, а также проведением флуоресцентной ангиографии и оптической когерентной томографии. При неоваскулярной форме макулярной дегенерации, а также в случае ассоциированной с патологической миопией хориоидальной неоваскуляризации отсутствие отрицательной динамики по остроте зрения и состоянию сетчатки считается мерой эффективности терапии. При отсутствии эффекта от нескольких введений Луцентиса врач вправе отменить терапию, не дожидаясь окончания курса лечения. Применение Луцентиса можно сочетать с лазерной коагуляцией сетчатки.
Интравитреальное введение Луцентиса
Интравитреальное введение Луцентиса является оперативным вмешательством на глазном яблоке, поэтому должно проводиться в стерильной операционной. Оптимальной профилактикой послеоперационных инфекционных осложнений является соблюдение всех правил асептики, а также обработка операционного поля йодсодержащим антисептиком, при отсутствии аллергической реакции на йод. Перед манипуляцией врач проводит осмотр глазного дня и измерение внутриглазного давления. Толщина иглы для интравитреального введения Луцентиса – 27-30G. Место введения располагается в 3,5-4 мм от лимба, в так называемом pars plana, чтобы не задеть сетчатку и хрусталик. После прохождения иглы в полость глазного яблока производится постепенное интравитреальное введение Луцентиса в стекловидное тело. Укол Луцентиса является практически безболезненным, поэтому местной анестезии в виде глазных капель или геля с анестетиком достаточно.
| Укол Луцентиса |
Контроль внутриглазного давления необходимо проводить в течение 30 минут после интравитреального введения Луцентиса. Также специалистом обязательно проводится контроль перфузии по ретинальной артерии. Через 3-7 дней после манипуляции необходим офтальмологический осмотр для контроля состояния глазного дна и раннего выявления инфекционных осложнений. Профилактическое введение антибиотика после интравитреального применения Луцентиса остается на усмотрение лечащего врача.
Противопоказания к введению Луцентиса
Противопоказания к применению описываемого препарата определяются не только свойствами самого лекарственного средства, но и методикой его использования. Существуют ситуации, когда само по себе интравитреальное введение Луцентиса противопоказано тому или иному пациенту. Применение Луцентиса противопоказано в следующих клинических ситуациях:
- Индивидуальная непереносимость или гиперчувствительность к ранибизумабу, ранее возникавшие аллергические реакции на введение данного препарата.
- Доказанные инфекционно-воспалительные процессы глазного яблока и периокулярной области.
- Беременность и период лактации также являются противопоказаниям к применению Луцентиса.
- Возраст пациента до 18 лет, поскольку научные исследования по применению Луцентиса у пациентов детского возраста не проводились.
Как и показания, так и противопоказания к интравитреальному введению Луцентса определяются лечащим врачом индивидуально для каждого пациента.
Препараты-аналоги Луцентиса
Группа антипролиферативных средств представлена не только Луцентисом. Существуют и другие препараты со схожим механизмом действия. Рассмотрим некоторые из них:
- Авастин. Действующим веществом данного препарата является бевацизумаб, который по механизму действия схож с ранибизумабом или Луцентисом. Авастин активно применялся с целью химиотерапевтического лечения онкологических заболеваний. Позже были проведены научные исследования и доказана эффективность Авастина, как антипролиферативного агента. Бевацизумаб применяется для терапии диабетической ретинопатии, хориоидальной неоваскуляризации и неоваскулярной макулярной дегенерации.
- Эйлеа. Действующее вещество данного препарата – афлиберцепт. Данное средство было одобрено для терапии патологии глазного дна в 2011 году. Показания к применению сходи с таковыми у Луцентиса. Особенностью данного средства является его способность связывать не только эндотелиальный сосудистый фактор роста, но и плацентарный фактор роста. Особенностью данного препарата является более продолжительное время действия.
| Авастин (бевацизумб) и препарат Эйлеа (афлиберцепт) |
Выбор препарата из группы антивазопролиферативных средств всегда остается за лечащим врачом. Пациента всегда подробно информируют обо всех особенностях, на основании полученной информации он дает согласие на интравитреальное введение Луцентиса или любого другого его аналога.
Луцентис. Цена и стоимость лечения
Цена лечения Луцентисом включает не только стоимость препарата, но и саму процедурой интравитреального введения. Данная процедура, несмотря на кажущуюся несложность, является не менее ответственной манипуляцией, чем другие разновидность вмешательств в офтальмологии. Существует риск развития инфекционных осложнений после введения препарата в полость глазного яблока. Поэтому подобная манипуляция должна проводиться только высококвалифицированным специалистом в условиях стерильности. Необходимость проведения интравитреального введения Луцентиса в специализированной операционной, а также использование большого количества расходных материалов и определяет стоимость применения Луцентиса. Цена препарата Луцентис в розничной аптечной сети России составляет 50000-52000 рублей. Стоимость интравитреального введения препарата колеблется в диапазоне 18000-25000 рублей. Также необходимо помнить о контрольных посещениях офтальмолога в процессе лечения, а также о назначаемых врачом диагностических манипуляциях.
Луцентис. Отзывы и рекомендации
Луцентис – один из современных и безопасных антивазопролиферативных агентов, применение которого успешно помогает остановить прогрессирование таких грозных офтальмологических заболеваний, как диабетическая ретинопатия и неоваскулярная (влажная) форма макулярной дегенерации. Применение Луцентиса имеет большое количество положительных отзывов как среди пациентов с патологией сетчатки, так и среди практикующих врачей-офтальмологов. Его использование помогло сохранить и улучшить зрение огромному количеству пациентов. И если Вам ранее выполнялся укол Луцентиса, будем признательны, если Вы оставите свой отзыв о препарате на нашем сайте на странице Отзывы. Ведь возможно, что именно Ваш опыт и отзыв о Луцентисе поспособствуют выбору других пациентов.
Главная Поиск
Различные способы поиска
Поиск по базе данных: 

Репозиторий OAI—PMH
Репозиторий Российская Офтальмология Онлайн по протоколу OAI-PMH
Конференции
Офтальмологические конференции и симпозиумы
Видео
Видео докладов
Поздравляем–>