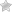Дистрофия сетчатки глаза возникает в следствии нарушения кровообращения и обменных процессов в тканях сетчатки глаза, что приводит к их отмиранию. Главной опасностью этого заболевания является то, что при несвоевременном лечении и доведении дистрофии до запущенной стадии пациент полностью теряет зрение.
Основными причинами возникновения дистрофии сетчатки глаза являются:
– нарушение работы сосудистой системы органа зрения и иммунной системы организма,
– хронические заболевания сердца и эндокринной системы,
– вредные привычки: алкоголь, курение, неправильное питание,
– хирургическое вмешательство или травмы глаз.
В зависимости от локализации дистрофии выделяют две ее разновидности:
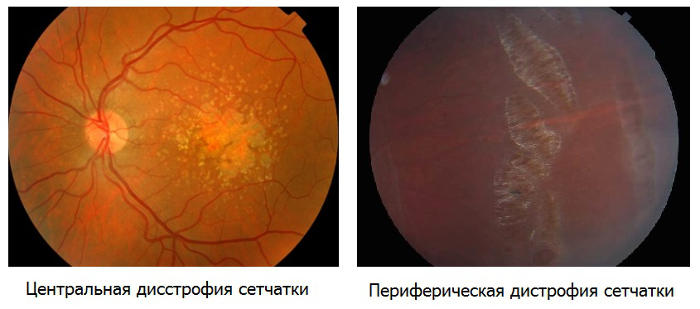
-
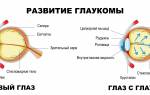
Периферическая дистрофия сетчатки глаза обычно является следствием перенесенной травмы глаза, воспалительного заболевания или близорукость, которая также является симптомом ранней стадии заболевания. При условии вовремя проведенной диагностики эта форма заболевания лечится хирургическим вмешательством.
-
При центральной дистрофии сетчатки разрушающий процесс происходит в молекулярной зоне глаза. Данная разновидность заболевания опасна тем, что процессы затрагивают центральную область глазного яблока, сложно поддаются лечению и приводит к потере зрения. Существуют две формы этой патологии: сухая и влажная.
При первой форме заболевания происходит накопление продуктов метаболизма зрительного органа между сетчаткой и сосудистой оболочкой. Вторая форма характеризуется образованием новых кровеносных сосудов, через которые к сетчатке поступает кровь и внутриглазная жидкость. Следствием этого процесса становится резкое снижение качества зрения, а при отсутствии лечение и полная потеря зрения.
Характерные признаки и симптомы
Ранние стадии дистрофии сетчатки протекают бессимптомно, с развитием заболевания проявляются следующие признаки:
-
появление вспышек и искр перед глазами;
-
сужение поля зрения;
-
снижение способности различать предметы в условиях плохой видимости;
-
ощущение пелены перед глазами;
-
нарушение резкости, искажение видимого;
-
метаморфопсия.
Эти симптомы могут сигнализировать о наличие многих заболеваний, поэтому при появлении хотя бы одного из них следует незамедлительно пройти полную диагностику зрительной системы. Это даст возможность обнаружить заболевание на ранней стадии и сохранить ваше зрение.
Диагностика дистрофии сетчатки
Для диагностики дистрофии сетчатки, определения стадии ее развития и назначения эффективного лечения необходимо пройти комплексную диагностику зрения, которая должна включать следующие обследования:

Периметрия – исследование поля зрения. Благодаря этому обследованию офтальмолог определят наличие сужения поля зрения, которое является одним из основных симптомов заболевания.
УЗИ органов зрения помимо полной картины состояния глазных мышц и зрительного нерва позволяет выявить патологические процессы и образовавшиеся опухоли в сетчатке.
Также важными обследованиями для определения состояния сетчатки глаза являются: измерение внутриглазного давления, биомикроскопия глаза, визометрия (оценка остроты зрения).
При необходимости получения дополнительных сведений офтальмолог может назначить дополнительные исследования, которые можно пройти в нашей клинике.
Диагностика зрительной системы в «Клинике микрохирургии «Глаз» имени академика С.Н.Федорова» проводится на оборудовании последнего поколения специалистами высшего класса. Это позволяет получить точные сведения о состоянии сетчатки и зрительной системы в целом и назначить своевременное лечение, что позволит сохранить ваше зрение.
Стоимость полной диагностики зрительной системы
Лечение дистрофии сетчатки
- Медикаментозная терапия
При условии вовремя проведенной диагностики и обнаружении дистрофии сетчатки на ранней стадии, возможно проведение медикаментозного лечения, которое будет оказывать воздействие на пораженную область сетчатки. Назначаемые препараты улучшают остроту зрения, лечат и питают витаминами пораженный орган.
Это вспомогательное лечение дистрофии, которое укрепляет мышечную систему глаза, стабилизирует внутриглазное давление. Физиотерапия при дистрофии сетчатки предусматривает несколько эффективных процедур: электростимуляция, фотостимуляция для тренировки внутренних возможностей, подключения резерва органа зрения, магнитотерапия, стимуляция лазерным излучением.
Все необходимые процедуры назначаются курсом и их можно пройти в нашей клинике. Кабинет физиолечения «Клиники микрохирургии «Глаз» имени академика С.Н.Федорова» оборудован современными аппаратами, что обеспечит эффективное лечение.
Стоимость физиолечения
- Укрепление сетчатки глаза лазером
Это эффективный метод остановить дистрофию, а для этого лазер разграничивает здоровые и пораженные ткани. Под его воздействием больные сосуды как бы «запаиваются», в результате чего по ним прекращается течение жидкости. Как следствие, расслоение сетчатки при дистрофии останавливается, болезнь перестает стремительно прогрессировать.
Подробнее о лазеркоагуляции сетчатки вы поможете прочесть здесь.
Стоимость лазеркоагуляции
Хирургическое вмешательство
Выбор такого лечения уместен, когда лазерная коррекция и медикаментозная терапия неэффективны, необходимы радикальные методы. Хирургическое вмешательство при прогрессирующей дистрофии может быть двух видов:
- Реваскуляризирующая операция предусматривает закупорку пораженных и увеличение просвета здоровых сосудов.
- Вазореконструктивная операция проходит с участием трансплантатов, которые помогают нормализовать микрососудистое русло глаза.
Дистрофия сетчатки является одной из причин ухудшения или полной потери зрения, она может долгое время ничем субъективно не проявляться, однако она ведет к необратимым изменениям.
Для снижения риска развития дистрофии сетчатки необходимо регулярно проходить полную диагностику зрительной системы, ежедневно делать гимнастику для глаз, носить солнцезащитные очки для избежания вредного воздействия ультрафиолетовых лучей на сетчатку, сбалансированно питаться и следить за состоянием своего зрения.
Коротко
Возрастная макулодистрофия — прогрессирующее хроническое заболевание сетчатки, которое, наряду с катарактой, открытоугольной глаукомой и диабетической ретинопатией, является ведущий причиной потери зрения и поражает большинство лиц в возрасте старше 50 лет. Патология характеризуется наличием друз (очаговые желтоватые отложения внеклеточного матрикса), географической атрофией пигментного эпителия сетчатки, ростом новых сосудов. Лечение разнится в зависимости от типа возрастной макулодистрофии, которая бывает сухой (атрофической, неэксудативной) и влажной (неоваскулярной, эксудативной).
«Беову» бросит серьезный вызов таким давно существующим препаратам против макулодистрофии, как «Эйлеа» (Eylea, афлиберцепт), за которым стоят «Ридженерон фармасьютикалс» (Regeneron Pharmaceuticals) и «Байер» (Bayer), и «Луцентис» (Lucentis, ранибизумаб) авторства «Рош» (Roche). Во-первых, бролуцизумаб характеризуется повышенной эффективностью лечения макулодистрофии, подтвержденной в ходе прямого сравнения с афлиберцептом; ранибизумаб уступает последнему. Во-вторых, инъекции «Беову» осуществляются реже, чем таковые для «Эйлеа» или «Луцентиса», что важно, поскольку интравитреальное введение препарата, то есть в стекловидное тело, является всё же травматической для органов зрения процедурой.
Подробности
Безопасность и эффективность бролуцизумаба были изучены в клинических испытаниях HAWK (NCT02307682) и HARRIER (NCT02434328) фазы III (рандомизированных, двойных слепых, с группой активного препарата, многоцентровых, международных) среди пациентов (n=1817) с прежде нелеченной активной хороидальной неоваскуляризацией, вторичной к возрастной макулодистрофии. Участникам назначали интравитреальные инъекции или бролуцизумаба, или афлиберцепта. Экспериментальный препарат в дозе 3 или 6 мг применялся по схеме каждые 8 или 12 недель после первых трех ежемесячных нагрузочных доз. Схема применения 2-мг дозы «Эйлеа» предполагала его инъекции каждые 8 недель после аналогичной нагрузки.
Что касается других анатомических и функциональных показателей, «Беову» удалось вырваться вперед, продемонстрировав более выраженное действие на сдерживание активности заболевания. Так, согласно оптической когерентной томографии, группы бролуцизумаба отметились меньшей пропорцией пациентов, столкнувшихся с интраретинальной (IRF), субретинальной (SRF) экссудацией и/или экссудацией под пигментный эпителий сетчатки (RPE) как феномена протекания кровеносных сосудов, влекущего за собой отслоение сетчатки. Бролуцизумаба также обеспечил усиленное уменьшение толщины центрального подполя (CST) сетчатки, отражающего патологическое накопление жидкости.
Основной проблемой бролуцизумаба является повышенная до 3–5% вероятность внутриглазного воспаления в форме: клеточной реакции влаги передней камеры, клеточной опалесценции в передней камере, воспаления в передней камере, хориоретинита, воспаления глаза, иридоциклита, иритита, увеита, помутнения стекловидного тела, витрита. Для сравнения: для «Эйлеа» и «Луцентиса» частота подобных побочных реакций составляет 0,01% и не более 0,6% соответственно.
«Мосмедпрепараты»
Кроме того, есть некоторые претензии к повышенной иммуногенности «Беову»: к нему, как и любому другому моноклональному антителу, в организме могут уже присутствовать антитела, титр которых в ходе назначения препарата растет. Антитела против бролуцизумаба были обнаружены у 36–52% пациентов до начала лечения и у 53–67% после. Возможно, столь высокий уровень связан с кроличьей природой гипервариабельного участка антитела (определяет его комплементарность), хотя последнее и прошло гуманизацию. Для сравнения: антитела против афлиберцепта и ранибизумаба изначально выявляются у 1–3% и 0–5% человек, по ходу лечения оставаясь на прежнем уровне для первого препарата и увеличиваясь до 1–9% пациентов для второго.
Бролуцизумаб (brolucizumab) — одноцепочечный фрагмент вариабельного домена (scFv) гуманизированного моноклонального антитела, ингибирующий фактор роста эндотелия сосудов A (VEGF-A) путем связывания с тремя его основными изоформами: VEGF110, VEGF121 и VEGF165. Подавление VEGF-A отражается сдерживанием пролиферации эндотелиальных клеток, неоваскуляризации и проницаемости сосудов. Благодаря небольшому размеру молекулы (26 кДа) оказалось возможным доставить увеличенную молярную дозу и обеспечить более эффективное тканевое проникновение, и в результате чего продлить терапевтическое действие.
Схема применения «Беову» обращается к нагрузочному периоду (одна ежемесячная инъекция в течение трех месяцев), а затем к поддерживающей терапии (одна инъекция раз в два-три месяца). Следует понимать, что применение «Беову» раз в квартал подтверждено клиническими испытаниями: по истечении года лечения свыше половины пациентов придерживались такого интервала дозирования (56% участников HAWK и 51% HARRIER), а по прошествии двух лет 45% и 39%.
«Эйлеа» назначается раз в два месяца после аналогичного нагрузочного периода. Да, с недавних пор афлиберцепт разрешено вводить реже — раз в три месяца, однако такая частота инъекций, во-первых, не столь эффективна и, во-вторых, допущена лишь после целого года терапии по стандартной схеме раз в два месяца. При этом рекомендовано на постоянной основе оценивать статус прогрессирования заболевания, дабы вовремя сократить интервал между дозами.
В 2017 году «Эйлеа» и «Луцентис», который вводится раз в месяц, заработали 5,93 и 3,30 млрд долларов, в 2018 году спрос на них вырос до 6,75 и 3,71 млрд долларов. К слову, права на реализацию «Луцентиса» за пределами США принадлежат «Новартис», которая поимела на нем 1,89 и 2,05 млрд долларов за два минувших года. Однако в 2020 году афлиберцепт потеряет патентную защиту в Европейском союзе, и срочно была нужна качественная замена.
«Новартис» весьма надеется на успех «Беову» — даром что ли швейцарский фармгигант истратил дорогостоящий ваучер на приоритетное рассмотрение регулятором: возрастная макулодистрофия продолжает захватывать всё новых пациентов ввиду равно как стареющего населения, так и отсутствия превентивных процедур. Но бролуцизумабу предстоит пройти долгий путь, прежде чем он сможет занять позицию вровень с конкурентами, располагающими, помимо влажной возрастной макулодистрофии, и рядом других показаний. Вот почему бролуцизумаб параллельно проходит не менее семи клинических испытаний фазы III, в которых напрямую сравнивается с афлиберцептом в терапии диабетического макулярного отека, макулярного отека ввиду окклюзии вен сетчатки, а также влажной возрастной макулодистрофии, не отзывающейся на применение VEGF-ингибиторов.
Впрочем, конкуренты не спят. Так, «Рош» доводит до ума фарицимаб (faricimab) — биспецифическое моноклональное антитело, связывающее и инактивирующее одновременно VEGF-A и ангиопоэтин-2 (Ang2). «Аллерган» (Allergan) и «Молекьюлар партнерс» (Molecular Partners) с заключительной проверкой абисипара (abicipar) — DARPin-соединения против VEGF-A. Однако у «Аптоутек» (Ophthotech) три раза кряду ничего не вышло с экспериментальным «Фовиста» (Fovista, пегплераниб), аптамером против фактора роста тромбоцитов (PDGF), но продолжается изучение прототипного «Зимура» (Zimura, авацинкаптад пегол), таргетированного на компонент 5 системы комплемента (C5). Интересным представляется KVD001, ингибитор плазменных калликреинов (PKal), тестируемый «Калвиста фармасьютикалс» (KalVista Pharmaceuticals) и «Мерк и Ко» (Merck & Co.).
В июле 2019 года «Новартис» успешно сделку с «Такеда фармасьютикал» (Takeda Pharmaceutical), в рамках которой японцы ввиду поглощения «Шайр» (Shire) продали «Зайдра» (Xiidra, лифитеграст) — блокатор взаимодействия между функционально связанным антигеном 1 лимфоцитов (LFA-1) и молекулой межклеточной адгезии 1 (ICAM-1), применяемый в терапии сухого кератоконъюнктивита (синдрома сухого глаза). Компания из Базеля за лифитеграст авансом 3,4 млрд долларов и пообещала еще до 1,9 млрд долларов по мере его продаж.
Ученые МФТИ в сотрудничестве с исследователями Гарварда вырастили клетки сетчатки, которые способны врастать в глаза. Это первая в мире успешная попытка трансплантации ганглионарных клеток (нейроны сетчатки, которые разрушаются при глаукоме), полученных из стволовых клеток в лабораторных условиях. Далее выращенные клетки нужно будет трансплантировать в сетчатку. Ученые проверили технологию на мышах и удостоверились в успешном встраивании клеток и их выживании на протяжении года. В дальнейшем исследователи планируют создать специализированные банки клеток, которые позволят индивидуально подбирать терапию для каждого пациента.
Операция «Трансплантация»
Первую в мире успешную попытку выращивания и трансплантации ганглионарных клеток сетчатки из стволовых произвели ученые лаборатории геномной инженерии МФТИ в сотрудничестве с исследователями Гарвардской медицинской школы. Ганглионарные клетки ответственны за передачу зрительной информации, и именно они повреждаются при глаукоме. Ученым удалось не только вырастить нейроны (ганглионары считаются специализированными нейронами), но и трансплантировать их в глаза мышей, добившись правильного врастания искусственной ткани сетчатки. Как известно, без лечения развитие глаукомы может привести к необратимому повреждению части зрительного нерва и, как следствие, потери части визуального поля. Прогрессируя в течение долгого времени, эта болезнь может привести и к полной слепоте.
В поле зрения: ученые открыли ген наследственной слепоты Болезнь вызывает мутация, из-за которой перестает вырабатываться важный белок
Клетки сетчатки были выращены в специальных органоидах, ткань формировалась в пробирке, рассказал «Известиям» младший научный сотрудник лаборатории геномной инженерии МФТИ Евгений Кегелес. Потом эти клетки пересадили мышам, которые были распределены в несколько групп.
— Были мыши с моделью глаукомы, мыши с повышенным внутриглазным давлением и те, у которых были удалены собственные ганглионары, — отметил Евгений Кегелес. — Были также новорожденные мыши: мы проверяли гипотезу более успешной приживаемости молодых ганглионарных клеток в формирующейся сетчатке. В результате оказалось, что клетки встроились и прорастили аксоны, которые позволят связать глаз с мозгом. Улучшенная выживаемость клеток у новорожденных мышей дает нам перспективное направление для поиска наилучшего микроокружения.
По словам Евгения Кегелеса, эти клетки успешно просуществовали внутри сетчатки 12 месяцев, что является серьезным сроком для такого исследования. Ученым удалось убедиться, что они получают зрительные сигналы, однако то, что клетки передают сигналы в мозг, со стопроцентной уверенностью утверждать пока нельзя.
— Мы точно знаем, что выращенные клетки встраиваются куда надо, протягивают аксоны в мозг, но их функциональность оценить пока невозможно, — объяснил Евгений Кегелес. — Это связано с тем, что до сих пор нам не удалось вырастить большое количество клеток. Это вопрос ближайших лет.
По его словам, исследователям нужен год, чтобы они смогли оценить функциональность клеток на мышиных моделях. В течение этого времени можно будет получить доказательство, что клетки не просто правильно встроены в структуру глаза, а они именно «видят».
Клеточный банк
Сейчас мышиные клетки сетчатки удается вырастить примерно за 21 день. В случае человека это будет от 50 до 100 дней, говорят ученые МФТИ.
Однако, скорее всего, человеку с глаукомой, готовящемуся к трансплантации, не нужно будет выращивать ткань сетчатки из собственных стволовых клеток. Так как глаз является иммунопривилегированным органом, где отторжения редки, возможно создать банк клеток для таких пациентов. Там будут размещены или выращенные клетки сетчатки от универсального донора, или из индуцированных плюрипотентных стволовых клеток. Это значит, что можно будет заранее вырастить клетки, заморозить их и, когда пациент с глаукомой обратится за помощью, подобрать для него наилучший клеточный вариант для трансплантации.
Земля не плоская: вернуть объемное зрение помогут компьютерные очки Разработанный российскими учеными прибор исправит серьезную патологию за несколько месяцев в домашних условиях
Впоследствии эту технологию можно будет применять и для лечения других заболеваний глаз, например дистрофии сетчатки. Однако выращивать придется другие клетки.
— Нобелевскую премию за индуцированные плюрипотентные стволовые клетки дали почти 10 лет назад, в 2012 году, — отметил руководитель лаборатории геномной инженерии Павел Волчков. — Так называемый хайп, когда буквально все научные коллективы считали своим долгом заниматься этой тематикой, давно угас. Сейчас настало время не просто слов, а реальных технологий на основе iPS (искусственные плюрипотентные стволовые клетки человека. — «Известия»). И именно к таким технологиям относится исследование по трансплантации ганглионаров сетчатки. Это возможность показать, что стволовые клетки реально можно применить на практике, с их помощью можно что-то исправить. Хотя эта работа еще не доведена до клиники, но она уже в нескольких шагах от реальной пересадки с целью лечения глаукомы.
Учитывая большой опыт экспериментальных работ мировых ученых и активное изучение вопроса заместительной клеточной терапии в офтальмологии, в дальнейшем метод может привести к прорыву в диагностике и лечении глаукомы, считает заведующая отделением офтальмологии ФГБУ НМИЦО ФМБА России, действительный член Европейского общества катарактальных и рефракционных хирургов (ESCRS), член Российского общества офтальмологов Ника Тахчиди.
Слепой метод: что помогает незрячим ориентироваться в телефоне и мире Прототипов сотни, реально доступных устройств — единицы
— В ряде зарубежных работ показано, что введенные клетки встраиваются в сетчатку и частично дифференцируются в клетки сетчатки. В настоящее время описаны и обсуждаются два основных механизма действия клеток in vivo и in vitro. Замещающая терапия — когда клетки, образующиеся в результате дифференцировки введенных стволовых клеток, «включаются» в восстанавливаемую ткань. «Эффект стороннего наблюдателя» — когда вводимые стволовые клетки оказывают противовоспалительное, трофическое или иммуномодулирующее действие на восстанавливаемую ткань. Однако, несмотря на прорыв в изучении морфофунциональных свойств стволовых клеток, обеспечить гарантированное послойное замещение культивированными клетками поврежденных участков сетчатки при использовании практикуемых методов введения на сегодняшний день невозможно, что и подтверждается рядом экспериментальных работ, — сказала Ника Тахчиди.
Впрочем, многие ученые в мире сейчас работают в этом направлении, пытаясь создать клеточную терапию лечения атрофии зрительного нерва, дистрофии сетчатки и глаукомы, отметила заведующая отделением офтальмологии клинико-диагностического центра «Медси», врач-офтальмолог Ирина Евсегнеева.
— Но никаких данных на сегодняшний день о том, что пересаженные клетки передают изображение, нет. Любая идея, как это сделать, заслуживает внимания, — сказала она.
По оценке ученых МФТИ, на доведение технологии до применения в лечебной практике уйдет примерно 10 лет.
Читайте также
Дистрофия сетчатки глаза – это серьезное заболевание, которое может приводить к полной и необратимой слепоте при отсутствии своевременно принятых мер.
Зачем лечить дистрофию?
Основой болезни является разрастание сосудов сетчатки. В дальнейшем происходит патологический рост соединительной ткани и нарушение кровообращения в данной области. Особенно выраженной клиническая симптоматика является при поражении области макулы, которая отвечает за точное зрение. Лечение дистрофии сетчатки зависит от причин, вызвавших ее.
В основе всех методов – воздействие на измененную сетчатую оболочку с целью остановить патологическое разрастание сосудов.
Лекарственные методы лечения сетчатки
В начальных стадиях для лечения используются препараты:
- антиоксиданты,
- улучшающие антиагрегантные свойства крови,
- стимулирующие кровообращение,
- нейропротекторные.
Эти средства могут приостановить дистрофический процесс и улучшить питание тканей сетчатой оболочки. Также существуют средства, которые вводятся непосредственно в глазное яблоко. Их действие основано на снижении активности фактора роста новообразованных сосудов на сетчатой оболочке.
Однако все лекарственные средства используются лишь в рамках поддерживающей терапии. Они не могут радикально решить проблему дистрофии.
Фотодинамическая терапия
Данная методика подразумевает внутривенное введение препарата, который проникает в новообразованные сосуды глазного яблока и закрепляется там. Кратковременное облучение глаз вызывает разрушение лекарственного вещества вместе с патологической сосудистой сетью.
Лазерное воздействие
Этот способ основан на использовании точечного лазерного излучения на сетчатую оболочку и представляет собой бескровное, нетравматичное и непродолжительное вмешательство.
Существует два метода:
- Транспупиллярная терапия. Этот способ лечения дистрофии сетчатки основан на применении слабого лазерного излучения широкой площади. Облучение при транспупиллярной терапии обладает относительно низкой энергией и не создает коагулятов, т. е. участков «припаивания». Однако такое воздействие оказывает положительное стимулирующее действие на глазное дно. Увеличивается активность клеток-фагоцитов, улучшается кровоснабжение и стимулируются антиоксидантные свойства сетчатой оболочки.
- Фокальная коагуляция. Данный метод используется при локализации дистрофических процессов преимущественно по периферии сетчатки, вне зоны макулы. Метод основан на создании точечных коагулятов, что позволяет снизить риск возникновения отслойки сетчатой оболочки.
Как обратиться в Центр глазной хирургии
Чтобы записаться на прием, можно позвонить по телефону +7(495)727-00-44 или использовать онлайн-форму.
Дистрофия сетчатки должна быть своевременно диагностирована: это поможет остановить прогрессирование болезни и избежать слепоты!
| Один разрыв | от 5000 |
| Один квадрант | 9000 |
| Четыре квадранта | 27500 |
| Панретинальная коагуляция сетчатки при диабете | 28000 |
| Панретинальная коагуляции сетчатки при диабете (дополнительно) | 9000 |
| Коагуляция сетчатки на оперированной отслойке сетчатки | 10500 |
| Барраж макулярной зоны сетчатки | 10500 |
Оглавление:
Симптомы возрастной макулярной дегенерации Макулодистрофия глаза: методы лечения Противопоказания Преимущества лечения в клинике Санта
Возрастная макулодистрофия – одно из распространенных заболеваний у пациентов после 50 лет. В основе патологии лежит нарушение питания сетчатки, в частности центральной ее зоны. Одна из причин таких изменений – старение, но немалая роль отводится и наследственности. Для лечения возрастной макулярной дегенерации в ход идут как традиционные, так и хирургические методы.
Возрастная макулодистрофия приводит к постепенной и безболезненной потере зрения. Пациент жалуется на затуманенность, которую не получается скорректировать путем подбора очков или линз, отсутствие различения оттенков тонов, размытые буквы при чтении.
Эти процессы происходят из-за поражения центра сетчатки – макулы, которая зовется еще желтым пятном. В этом месте находится наибольшее количество фоторецепторов, и она отвечает за предметное зрение.
С возрастом между сетчаткой и сосудистой оболочкой глаза откладываются продукты жизнедеятельности – друзы. Они формируются из-за плохого питания тканей и замедленного выведения продуктов обмена. Избыточное количество друз приводит к тому, что пигментный эпителий и фоторецепторы повреждаются. Процесс еще больше усугубляется под воздействием ультрафиолетовых лучей.
Далее развивается одна из форм патологии: сухая или влажная. Сухая макулодистрофия характеризуется отложением друз между пигментным эпителием и мембраной Бруха – барьером между сетчаткой и сосудистой оболочкой. У пациента снижается центральное зрение, особенно при слабом свете или в сумерках. Болезнь может остановиться в своем развитии на несколько лет или переходить в другие формы.
Влажная, или экссудативная макулодистрофия развивается вследствие разрастания сосудов – неоваскуляризации. Эта форма заболевания считается более агрессивной и ведет к стремительной потере зрения. Пациент жалуется на появление перед глазом серого пятна, искривленное восприятие предметов. При влажной макулодистрофии новообразованные сосуды проникают в субретинальное пространство, разрушают мембрану Бруха и образуют сосудистую сеть.
Через нее под центральную область сетчатки просачиваются элементы крови, жидкости. Эти процессы сопровождаются кровоизлияниями в макулу. Мембрана Бруха, фоторецепторы и пигментный эпителий отделяются друг от друга. Постепенно в области макулы формируется валик, окруженный рубцовой тканью. Влажная форма развивается быстро и за несколько месяцев или недель может привести к потере зрения.
Независимо от разновидности патологии, можно выделить общую, характерную для обоих видов симптоматику:
- снижение предметного зрения с появлением в центральной зоне черного или серого пятна;
- проблемы с чтением и письмом, распознаванием лиц, вождением авто;
- трудности с дифференциацией цветов и их оттенков;
- нарушения в восприятии расстояний, изменения текстуры окружающих предметов;
- необходимость в большем уровне освещения.
Появление этих симптомов указывает на возрастную макулярную дегенерацию, для лечения которой нужно сразу обратиться к офтальмологу.
Лечение возрастной дегенерации в Челябинске в клинике Санта невозможно без предварительной диагностики. Начинается она с осмотра глазного дна. Обязательными исследованиями являются тест Амслера, флюоресцентная ангиография, оптическая когерентная томография.
При сухой форме макулодистрофии рекомендуется антиоксидантная терапия, бады, витаминно-минеральные комплексы. С помощью этих методов приводится в норму обмен веществ и увеличивается антиоксидантная защита сетчатки.
Один из наиболее действенных способов лечения возрастной макулярной дегенерации – интравитреальные введения антиангиогенных препаратов. Этот метод больше подходит для терапии влажной формы патологии. Медикаменты ставят блок на сосудистом факторе роста, подавляя процесс субретинальной неоваскуляризации. Антиангиогенные препараты стабилизируют и улучшают зрительные функции. Основной недостаток метода – быстрое снижение эффекта при отказе от данного способа лечения.
Для лечения влажной макулодистрофии глаза могут быть показаны лазерные методики. Их цель – прекращение кровотока в новообразованных сосудах путем их коагуляции лазерным лучом. Но этот метод имеет ряд ограничений, связанным с высоким риском повреждения фоторецепторов.
Альтернатива лазерному лечению – фотодинамическая терапия. Лазер воздействует на новообразованные сосуды и блокирует в них кровоток, при этом применяется светочувствительный препарат, накапливаемый только в области неоваскуляризации. Под воздействием лазерного излучения он приводит к формированию тромба и останавливает кровоток. В ходе фотодинамической терапии воздействие происходит только на сосуды, фоторецепторы остаются нетронутыми.
Транспупиллярная термотерапия – метод, который хорошо зарекомендовал себя при лечении влажной формы. Это альтернатива фотодинамической терапии. В ходе манипуляций происходит облучение инфракрасным лазером, уменьшающее кровоток в сосудистой оболочке глаза, не затрагивая фоторецепторы.
Хирургическое лечение возрастной дегенерации сетчатки проводится в при тяжелых стадиях патологии. Показаниями могут быть множественные субретинальные кровоизлияния при влажной форме заболевания. Популярный метод оперативного вмешательства – витрэктомия, в ходе которой стекловидное тело иссекается для обеспечения доступа к сетчатке.
Макулярная дистрофия – заболевание, которое трудно поддается лечению. Чем быстрее оно будет начато, тем легче добиться улучшение зрения. Важно регулярно проходить осмотр у офтальмолога, чтобы предупредить развитие патологии.
Для каждого из перечисленных методов лечения макулодистрофии существуют свои противопоказания. Но есть и заболевания, при которых опасна любая из перечисленных методик:
- онкология;
- нарушения свертываемости крови;
- тяжелые соматические состояния;
- отсутствие светоощущения.
Выбор каким методом лечить возрастную макулодистрофию осуществляется офтальмологом после проведения комплексного обследования пациента с учетом выявленных противопоказаний.
Пройти обследование и лечение возрастной макулярной дегенерации можно в клинике Санта в Челябинске. У нас работают квалифицированные специалисты, которые уже провели сотни сложных операций и регулярно повышают свой профессиональный уровень.
К каждому пациенту при возрастной макулодистрофии осуществляется индивидуальный подход. Врач внимательно выслушивает жалобы, расспрашивает об особенностях организма. Диагноз возрастная макулодистрофия ставится после детального осмотра. При необходимости офтальмолог отправляет пациента к другим специалистам узкого профиля. Выбор метода лечения проводится с согласованием с пациентом после получения результатов анализа.
Благодаря опыту и квалификации наших офтальмологов вы сможете вернуть себе зрение при возрастной макулодистрофии и возможность увидеть мир четким и ярким. Записывайтесь на прием по телефону: операторы подберут для визита комфортное для вас время.