Содержание
- Операция «Трансплантация»
- Клеточный банк
- История создания зрительного протеза
- Первые ретинальные импланты
- Тренды ретинальных имплантов: основные фундаментальные технологии
- Российский опыт ретинального протезирования
- Кортикальные системы имплантации
- Почему сетчатка у человека не восстанавливается?
- Читать статьи по темам:
Ученые МФТИ в сотрудничестве с исследователями Гарварда вырастили клетки сетчатки, которые способны врастать в глаза. Это первая в мире успешная попытка трансплантации ганглионарных клеток (нейроны сетчатки, которые разрушаются при глаукоме), полученных из стволовых клеток в лабораторных условиях. Далее выращенные клетки нужно будет трансплантировать в сетчатку. Ученые проверили технологию на мышах и удостоверились в успешном встраивании клеток и их выживании на протяжении года. В дальнейшем исследователи планируют создать специализированные банки клеток, которые позволят индивидуально подбирать терапию для каждого пациента.
Операция «Трансплантация»
Первую в мире успешную попытку выращивания и трансплантации ганглионарных клеток сетчатки из стволовых произвели ученые лаборатории геномной инженерии МФТИ в сотрудничестве с исследователями Гарвардской медицинской школы. Ганглионарные клетки ответственны за передачу зрительной информации, и именно они повреждаются при глаукоме. Ученым удалось не только вырастить нейроны (ганглионары считаются специализированными нейронами), но и трансплантировать их в глаза мышей, добившись правильного врастания искусственной ткани сетчатки. Как известно, без лечения развитие глаукомы может привести к необратимому повреждению части зрительного нерва и, как следствие, потери части визуального поля. Прогрессируя в течение долгого времени, эта болезнь может привести и к полной слепоте.

Клетки сетчатки были выращены в специальных органоидах, ткань формировалась в пробирке, рассказал «Известиям» младший научный сотрудник лаборатории геномной инженерии МФТИ Евгений Кегелес. Потом эти клетки пересадили мышам, которые были распределены в несколько групп.
— Были мыши с моделью глаукомы, мыши с повышенным внутриглазным давлением и те, у которых были удалены собственные ганглионары, — отметил Евгений Кегелес. — Были также новорожденные мыши: мы проверяли гипотезу более успешной приживаемости молодых ганглионарных клеток в формирующейся сетчатке. В результате оказалось, что клетки встроились и прорастили аксоны, которые позволят связать глаз с мозгом. Улучшенная выживаемость клеток у новорожденных мышей дает нам перспективное направление для поиска наилучшего микроокружения.
По словам Евгения Кегелеса, эти клетки успешно просуществовали внутри сетчатки 12 месяцев, что является серьезным сроком для такого исследования. Ученым удалось убедиться, что они получают зрительные сигналы, однако то, что клетки передают сигналы в мозг, со стопроцентной уверенностью утверждать пока нельзя.
— Мы точно знаем, что выращенные клетки встраиваются куда надо, протягивают аксоны в мозг, но их функциональность оценить пока невозможно, — объяснил Евгений Кегелес. — Это связано с тем, что до сих пор нам не удалось вырастить большое количество клеток. Это вопрос ближайших лет.
По его словам, исследователям нужен год, чтобы они смогли оценить функциональность клеток на мышиных моделях. В течение этого времени можно будет получить доказательство, что клетки не просто правильно встроены в структуру глаза, а они именно «видят».
Клеточный банк
Сейчас мышиные клетки сетчатки удается вырастить примерно за 21 день. В случае человека это будет от 50 до 100 дней, говорят ученые МФТИ.
Однако, скорее всего, человеку с глаукомой, готовящемуся к трансплантации, не нужно будет выращивать ткань сетчатки из собственных стволовых клеток. Так как глаз является иммунопривилегированным органом, где отторжения редки, возможно создать банк клеток для таких пациентов. Там будут размещены или выращенные клетки сетчатки от универсального донора, или из индуцированных плюрипотентных стволовых клеток. Это значит, что можно будет заранее вырастить клетки, заморозить их и, когда пациент с глаукомой обратится за помощью, подобрать для него наилучший клеточный вариант для трансплантации.

Впоследствии эту технологию можно будет применять и для лечения других заболеваний глаз, например дистрофии сетчатки. Однако выращивать придется другие клетки.
— Нобелевскую премию за индуцированные плюрипотентные стволовые клетки дали почти 10 лет назад, в 2012 году, — отметил руководитель лаборатории геномной инженерии Павел Волчков. — Так называемый хайп, когда буквально все научные коллективы считали своим долгом заниматься этой тематикой, давно угас. Сейчас настало время не просто слов, а реальных технологий на основе iPS (искусственные плюрипотентные стволовые клетки человека. — «Известия»). И именно к таким технологиям относится исследование по трансплантации ганглионаров сетчатки. Это возможность показать, что стволовые клетки реально можно применить на практике, с их помощью можно что-то исправить. Хотя эта работа еще не доведена до клиники, но она уже в нескольких шагах от реальной пересадки с целью лечения глаукомы.
Учитывая большой опыт экспериментальных работ мировых ученых и активное изучение вопроса заместительной клеточной терапии в офтальмологии, в дальнейшем метод может привести к прорыву в диагностике и лечении глаукомы, считает заведующая отделением офтальмологии ФГБУ НМИЦО ФМБА России, действительный член Европейского общества катарактальных и рефракционных хирургов (ESCRS), член Российского общества офтальмологов Ника Тахчиди.
Слепой метод: что помогает незрячим ориентироваться в телефоне и мире Прототипов сотни, реально доступных устройств — единицы
— В ряде зарубежных работ показано, что введенные клетки встраиваются в сетчатку и частично дифференцируются в клетки сетчатки. В настоящее время описаны и обсуждаются два основных механизма действия клеток in vivo и in vitro. Замещающая терапия — когда клетки, образующиеся в результате дифференцировки введенных стволовых клеток, «включаются» в восстанавливаемую ткань. «Эффект стороннего наблюдателя» — когда вводимые стволовые клетки оказывают противовоспалительное, трофическое или иммуномодулирующее действие на восстанавливаемую ткань. Однако, несмотря на прорыв в изучении морфофунциональных свойств стволовых клеток, обеспечить гарантированное послойное замещение культивированными клетками поврежденных участков сетчатки при использовании практикуемых методов введения на сегодняшний день невозможно, что и подтверждается рядом экспериментальных работ, — сказала Ника Тахчиди.
Впрочем, многие ученые в мире сейчас работают в этом направлении, пытаясь создать клеточную терапию лечения атрофии зрительного нерва, дистрофии сетчатки и глаукомы, отметила заведующая отделением офтальмологии клинико-диагностического центра «Медси», врач-офтальмолог Ирина Евсегнеева.
— Но никаких данных на сегодняшний день о том, что пересаженные клетки передают изображение, нет. Любая идея, как это сделать, заслуживает внимания, — сказала она.
По оценке ученых МФТИ, на доведение технологии до применения в лечебной практике уйдет примерно 10 лет.
Читайте также Порядка 40 млн слепых людей во всем мире нуждаются в технологиях, которые могут вернуть способность видеть. Однако до сих пор не существует доступного способа протезирования зрения
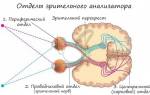
Мы привыкли ассоциировать зрение лишь с глазами. Однако помимо самих глазных яблок в процессе участвует зрительная кора головного мозга, которой мы фактически «видим», и нервные пути, которые соединяют глаза с мозгом. Практически на каждом этапе можно попытаться реализовать протезирование.
История создания зрительного протеза
Немецкий психолог Иоганн Пуркинье в 1823 году заинтересовался вопросами зрения и галлюцинаций, а также возможностью искусственной стимуляции зрительных образов. Принято считать, что именно он впервые описал зрительные вспышки — фосфены, которые он получил при проведении простого опыта c аккумулятором, пропуская через голову электрический ток и описывая свой визуальный опыт.
Спустя 130 лет, в 1956 году, австралийский ученый Дж. И. Тассикер запатентовал первый ретинальный имплант, который не давал какого-то полезного зрения, но показал, что можно искусственно вызывать зрительные сигналы.
Ретинальный имплант (имплант сетчатки) «вводит» визуальную информацию в сетчатку, электрически стимулируя выжившие нейроны сетчатки. Пока вызванные зрительные восприятия имели довольно низкое разрешение, но достаточное для распознавания простых объектов.
Но глазное протезирование долго тормозилось из-за технологических ограничений. Прошло очень много времени, прежде чем появились какие-то реальные разработки, которые смогли дать «полезное зрение», то есть зрение, которым человек мог бы воспользоваться. В 2019 году в мире насчитывалось около 50 активных проектов, фокусирующихся на протезировании зрения.
Первые ретинальные импланты
Пару лет назад на рынке было доступно три ретинальных импланта, которые прошли клинические испытания и были сертифицированы государственными регулирующими органами: европейским CE Mark и американским FDA.
- Second Sight Medical Products, США
- Pixium Vision, Франция
- Retina Implant AG, Германия
Так выглядели первые ретинальные импланты
Бионические импланты — это целая система внешних и внутренних устройств.
IRIS II (Pixium Vision) и Argus II (Second Sight) имели внешние устройства (очки с видеокамерой и блок обработки видеосигнала). Слепой человек смотрит при помощи камеры, с нее картинка направляется в процессор, где изображение обрабатывается и распадается на 60 пикселей (для системы Argus II). Затем сигнал направляется через трансмиттер на электродную решетку, вживленную на сетчатке, и электрическим током стимулируются оставшиеся живые клетки.
В немецком импланте Alfa АMS (Retina Implant) нет внешних устройств, и человек видит своим собственным глазом. Имплант на 1600 электродов вживляется под сетчатку. Свет через глаз попадает на светочувствительные элементы и происходит стимуляция током. Питается имплант от подкожного магнитного коннектора.
Субретинальный имплантат Alpha AMS компании Retina Implant AG
Все три ретинальных импланта больше не производятся, так как появилось новое поколение кортикальных протезов (для стимуляции коры головного мозга, а не сетчатки глаза). Однако хотя проектов по фундаментальным разработкам по улучшению ретинальных имплантов еще много, ни один из них не прошел клинические испытания:
- Улучшенный имплант DRY AMD PRIMA компании Pixium с увеличением количества электродов для стимуляции большего количества клеток сетчатки проходит клинические испытания. Для участия в программе испытаний еще ищут пять кандидатов;
- Retina Implant AG закрыли производство;
- Second Sight проводят клинические испытания своего кортикального импланта, но в марте 2020 года компания уволила 80% сотрудников из эксплуатационно-производственного подразделения.
Тренды ретинальных имплантов: основные фундаментальные технологии
Ретинальные нанотрубки
Группа ученых из Китая (Shanghai Public Health Clinical Center) в 2018 году провела эксперимент на мышах, в ходе которого вместо не функционирующих фоторецепторов сетчатки предложила использовать нанотрубки. Преимущество этого проекта — маленький размер нанотрубок. Каждая из них может стимулировать только несколько клеток сетчатки.
Биопиксели
Группа ученых из Оксфорда стремится сделать протез максимально приближенным к естественной сетчатке. Биопиксели в проекте выполняют функцию, схожую с настоящими клетками. Они имеют оболочку из липидного слоя, в который встроены фоточувствительные белки. На них воздействуют кванты света и как в настоящих клетках изменяется электрический потенциал, возникает электрический сигнал.
Перовскитная искусственная сетчатка
Все предыдущие фундаментальные разработки направлены на стимулирование всех слоев живых клеток. При помощи технологии перовскитной искусственной сетчатки китайские ученые пытаются предоставить возможность не только получать световые ощущения, но и различать цвет за счет моделирования сигнала таким образом, чтобы он воспринимался мозгом как имеющий определенную цветность.
Фотогальваническая пленка Polyretina
В Polyretina используется маленькая пленка, покрытая слоем химического вещества, которое имеет свойство поглощать свет и конвертировать его в электрический сигнал. Пленка размещена на сферическом основании, чтобы можно было удобно разместить ее на глазном дне.
Фотогальванический имплант Polyretina
Субретинальное введение полупроводникового полимера
Итальянские ученые предлагают технологию введения полупроводникового полимерного раствора под сетчатку, при помощи которого свет фиксируется и трансформируется в электрические сигналы.
Российский опыт ретинального протезирования
В России в 2017 году при поддержке фондов «Со-единение» и «Искусство, Наука и Спорт» было приобретено и установлено два ретинальных импланта Argus II американской компании Second Sight. Это единственные операции по восстановлению зрения, которые были проведены в России за все время. Каждая операция вместе с реабилитацией стоила порядка 10 млн руб, а сама система имплантации для одного пациента — порядка $140 тыс. Все прошло успешно, и два полностью слепых жителя Челябинска — Григорий (не видел 20 лет) и Антонина (не видела 10 лет) — получили предметное зрение. Предметное зрение означает, что человек может видеть очертания предметов — дверь, окно, тарелку — без деталей. Читать и использовать смартфон они не могут. Оба пациента имели диагноз «пигментный ретинит» (куриная слепота).
На момент 2019 года в мире установлено около 350 имплантов, произведенных компанией Second Sight. Около 50 тысяч россиян нуждаются в подобном протезе сетчатки.
В России опытом в протезировании зрения может похвастаться лишь один проект — АНО Лаборатория «Сенсор-Тех».
«Трендом в фундаментальных разработках бионических протезов является стремление сделать их максимально безопасными, приближенными к биологическим тканям людей и с максимально возможным разрешением. Но настоящую революцию вызвали кортикальные импланты, и смысл в ретинальных имплантах пропал, так как они ставятся только при пигментном ретините и возрастной макулярной дегенерации при отсутствии ряда противопоказаний. Кортикальные же импланты значительно расширяют горизонт показаний и позволяют восстанавливать полезное зрение даже людям, вовсе лишенным глаз», — рассказал Андрей Демчинский, к.м.н., руководитель медицинских проектов АНО Лаборатория «Сенсор-Тех».
Кортикальные системы имплантации
Кортикальные протезы — это подгруппа визуальных нейропротезов, способных вызывать зрительные восприятия у слепых людей посредством прямой электрической стимуляции затылочной коры мозга, которая отвечает за распознавание изображений. Этот подход может быть единственным доступным лечением слепоты, вызванной глаукомой, терминальной стадией пигментного ретинита, атрофией зрительного нерва, травмой сетчатки, зрительных нервов и т.п. За последние пять лет ученые решили задачу создания такого внутрикортикального визуального нейропротеза, с помощью которого можно было бы восстановить ограниченное, но полезное зрение.
В 1968 году Г.С. Бридли и В.С. Левин провели первую операцию по установке кортикальных имплантов. Первый имплант состоял из шапочки с коннекторами (устанавливали на череп под кожу) и отдельной дуги с электродами (устанавливали под череп), которые стимулировали кору головного мозга. Эксперимент был проведен на двух добровольцах для оценки возможности получения полезного зрения. Позднее импланты были извлечены. Технология кортикальных имплантов была заморожена по причине провоцирования приступов эпилепсии при стимуляции большего количества клеток мозга.
Первый кортикальный имплант
Кортикальный имплант Orion
Спустя 45 лет американский лидер разработки ретинальных имплантов Second Sight создал кортикальную протезную систему ORION. В конце 2017 года Second Sight получили разрешение от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) на проведение клинических испытаний. До апреля 2018 года было установлено шесть устройств. По результатам испытаний оказалось, что все пациенты ощущали зрительные стимулы, a у трех пациентов результаты были схожи с ретинальным имплантом Argus II и дали полезное предметное зрение. Клинические испытания будут проходить до июня 2023 года. Обязательным условием установки импланта является наличие у пациента зрительного опыта, то есть он может использоваться только для людей со сформированной зрительной корой, которые родились зрячими и потеряли зрение.
Система кортикальной имплантации Orion компании Second Sight
Кортикальный нейропротез CORTIVIS
Испанские ученые разработали кортикальный имплант под названием CORVITIS. Протез состоит из нескольких компонентов. Одна или две камеры обеспечивают получение изображения, которое затем обрабатывается биопроцессором, чтобы преобразовать визуальный образ в электрические сигналы. На втором этапе информация сводится в серию изображений и передается по радиочастотной связи на имплантированное устройство. Этот радиочастотный блок обеспечивает беспроводную передачу питания и данных во внутреннюю систему. Имплантированный электронный блок декодирует сигналы, определяет и контролирует форму напряжения и амплитуду формы волны, которая будет подаваться на соответствующие электроды. Клинические испытания на пяти пациентах завершатся в мае 2023 года.
Кортикальный имплант CORVITIS
Интракортикальный зрительный протез (WFMA)
Американские ученые разработали технологию многоканальной внутрикортикальной стимуляции с помощью беспроводных массивов металлических микроэлектродов и создали беспроводную плавающую микроэлектродную решетку (WFMA).
Система протеза состоит из группы миниатюрных беспроводных имплантируемых решеток-стимуляторов, которые могут передавать информацию об изображении, снятом на встроенную в очки видеокамеру, непосредственно в мозг человека. Каждая решетка получает питание и цифровые команды по беспроводной связи, так что никакие провода или разъемы не пересекают кожу головы. Посылая команды в WFMA, изображения с камеры передаются непосредственно в мозг, создавая грубое предметное визуальное восприятие изображения. Хотя восприятие не будет похоже на нормальное зрение, с его помощью человек может вести самостоятельную деятельность. Система ICVP получила одобрение FDA для проведения клинических испытаний.
Интракортикальный зрительный протез (WFMA)
Кортикальный протез NESTOR
Голландские ученые также разработали схожую технологию системы протезирования. Принцип функционирования протеза такой же, как в проектах выше. Камера отправляет сигнал на имплант, который состоит из тысяч электродов и смарт-чипа. С помощью процессора зрительное восприятие можно контролировать и регулировать.
«Хотя полное восстановление зрения пока кажется невозможным, кортикальные системы создают по-настоящему значимые визуальные восприятия, при помощи которых слепые люди могут распознавать, локализировать и брать предметы, а также ориентироваться в незнакомой среде. Результат — в существенном повышении уровня жизни слепых и слабовидящих. Такие вспомогательные устройства уже позволили тысячам глухих пациентов слышать звуки и приобретать языковые способности, и такая же надежда существует в области визуальной реабилитации», — обнадежил Андрей Демчинский.
Обновлено 14.08.2020
Ещё десятилетия назад заболевания сетчатки – ретинопатия, отслойка, дегенерация – приводили к слепоте. Современная офтальмология достигла такого уровня, когда возможно восстановление целостности сетчатки и её клеток.
Содержание статьи:
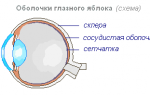
- Как устроена сетчатка глаза?
- Операции на сетчатке – показания к проведению и результаты
- Виды операций на сетчатке
- Восстановление после операций на глазу
- Мировой опыт в пересадке сетчатки – новое в хирургии глаза
- Стоимость операций на сетчатке за границей
- Как проводятся операции на сетчатке за рубежом
- Операции на сетчатке в Израиле
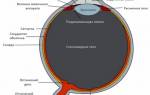
Способность видеть – прекрасное и не очень – это уникальный дар природы, связывающий нас с окружающим миром. Однако около 40 миллионов людей в мире лишены этой возможности, и основной причиной тому являются заболевания сетчатки глаз. Сетчатка – это главный элемент глаза, без которого зрение невозможно, даже при идеальном состоянии других элементов глаза. Это – особая оболочка, находящаяся сзади глаза, в области его дна, куда направляются все световые потоки через зрачок и прозрачные элементы глаза. После обработки световой информации сигналы (импульсы) передаются в зрительный нерв и по нём – в зрительный центр мозга, где формируется изображение, образы предметов.
Вмешательства на сетчатке глаза требуют различные её заболевания, не поддающиеся консервативному лечению за границей:
- лечение опухолей глаза за рубежом;
- лечение внутриглазной опухоли за границей;
- тяжёлые повреждения глаз;
- отслойка сетчатки;
- кровоизлияния в области макулы (центральной части сетчатки);
- макулодистрофия;
- отверстия и плёнки в макуле;
- диабетическая ретинопатия с участками отслойки, кровоизлияниями;
- воспаление и отёк макулы, не поддающиеся консервативному лечению.
Основное количество операций на сетчатке проводится для лечение отслоения сетчатки глаза.
- Операция экстрасклеральное пломбирование
Любая операция по лечению отслоения сетчатки направлена на то, чтобы уменьшить расстояние между сетчаткой и эпителием. В ходе операция экстрасклерального пломбирования определяют точное место отслоения, изготовляют пломбу нужного размера, накладывают ее на скалеру и фиксируют швами. При необходимости производится удаление скопившейс жидкости.
Полное восстановление после такой операции происходит в течение 2-3 месяцев. У пожилых пациентов – 3-4 месяца.
- Особенности операции экстрасклеральное баллонирование в лечении отслоения сетчатки глаза
Экстрасклеральное баллонирование проводится при неосложненных случаях отслоения сетчатки. Если есть значительные разрвы, то данный вид операции не проводится.
Во время операции за глаз вводится специальный баллон с катетером. В него нагнетается жидкость, которая расширяясь давит на склеру. Дополнительно проводят лазерокоагуляцию для укрепления оболочки. Успешность метода составляет 97%.
- Витрэктомия – для лечения отслойки сетчатки глаза
Витрэктомия – частичное или полное удаление стекловидного тела с дальнейшей заменой его на искусственный полимер, масло, солевой расствор или пузырьки с газом. Через проколы удаляют ткани стекловидного тела, прижигают лазером участки сетчатки, восстанавливают целостность сетчатки. Успешность такой операции составляет порядка 90%. Заживление проходит за 2-3 месяца переносится пациентами очень хорошо.
Восстаносительный процесс после операций на глазу зависит от многих факторов:
- Длительность операции
- Вид операции
- Тип заболевания
- Вид предварительного лечения
- Возраст пациента.
Среднее время полного восстановления составляет от двух до шести месяцев. Сушествует ряд общих реккомендаций, которые стоит соблюдать в послеоперационный период:
- Исключить тяжелый физический труд
- Соблюдать в начале постельный, а потом полупостельный режим
- Бережно относиться к глазам
- Применять противоспалительные капли
Некоторые заболевания пока что не поддаются лечению в рамках современной медицины. Но врачи никогда не останавливаются на достигнутом. Например, уже несколько лет ведутся непрерывные исследования в области пересадки сетчатки глаза. Пересадить сетчатку пока что не удалось, но был проведен ряд операций по пересадке искусственной сетчатки, которая представляла собой пронизанный электродами протез. Электроды имитировали работу нейронов и фоторецепторов, отправляли сигналы в мозг. Конечно, это не полноценная замена 120 миллионов зрительных рецепторов, но это огромный шаг вперед в мировой офтальмологии.
Проведение операций на сетчатке – это сложное мероприятие, требующее и высочайшей квалификации специалистов, и больших затрат времени, и дорогостоящих технологий. Поэтому и стоимость операций на сетчатке пока остаётся высокой, но она оправдывает результат, когда нет других способов восстановления зрения. И, тем не менее, у пациента есть выбор, потому что цены на операции в разных странах различны. Например, кто-то имеет достаточно средств для операции в США или Швейцарии, а очень многие выбирают операции на сетчатке в Израиле и Германии из-за более умеренных цен, по сравнению со странами запада. Стоимость лечения в Израиле будет самой низкой.
Ознакомиться со стоимостью различных операций можно на нашем сайте, связавшись с нами по контактному телефону, или заполнив форму обратной связи.
Не секрет, что многие пациенты с патологией сетчатки едут оперироваться в зарубежные клиники, и нередко – по рекомендации своего же лечащего врача, который честно заявляет, что современные технологии пока ещё доступны лишь в немногих клиниках, где огромные очереди в ожидании операции. В странах с развитой медициной проведение операций на сетчатке доступно во всех офтальмологических клиниках, и пациент может быстро получить самую квалифицированную помощь, на самом высоком уровне. Наиболее посещаемы постсоветскими пациентами клиники Германии и Израиля, где наряду с отличным качеством и профессионализмом стоимость лечения умеренна.
Операции на сетчатке в Германии базируются на новейшем офтальмологическом оборудовании, как для исследования глаза, так и для операций. Для исследования сетчатки применяются новейшие методы:
- HRT- ретинотомография,
- флюоресцентная ангиоретинография,
- метод IOL-мастер,
- когерентная томография.
Наиболее часто специалистам приходится сталкиваться с лечением отслойки сетчатки. Применяются различные лазерные и микрохирургические технологии, в комбинации с интравитреальным введением сосудистых и других препаратов. По показаниям выполняется удаление стекловидного тела с заменой его синтетической гелевой субстанцией. Особенно эффективна методика лечения диабетической ретинопатии, которая состоит в сочетании воздействия лазером с введением стероидного препарата Anti-VEGF. Профессионально выполняется удаление опухолей сетчатки при лечении рака за рубежом – лазерной и криогенная деструкцией, радиотерапией.
Операции на сетчатке глаза проводятся пактически во всех загарничных медицинских центрах. Если клиника имеет отделение офтальмологии, то проведение такого рода операций – это лицо клиники.
Большим спросом в мире пользуются операции на сетчатке в клиниках Израиля.
Вмешательства на сетчатке проводятся по двум методам:
- Экстрасклеральными методами создаётся участок вдавления на склере, который передаёт давление на сетчатку и препятствует её отслойке.
- Эндовитреальные вмешательства осуществляются через зрачок, с прохождением стекловидного тела. При этом используется электронная микроскопическая техника.
Выполняют лазерную фотокоагуляцию или криоретинопексию (сверхнизкой температурой). Удаляются образовавшиеся тяжи и плёнки, изменённое стекловидное тело с заменой его силиконовым гелем. Применяются различные модификации методов, появляются инновации. Одной из последних является технология восстановления клеток сетчатки методом оптогенетики с использованием белков водорослей и лазерного света. Израиль сегодня является признанным мировым лидером в профилактике и лечении слепоты. Это обязательно нужно учитывать тем, кому предстоит операция на сетчатке.
Появилась отдельная отрасль – хирургия сетчатки глаза. Сегодня операции на сетчатке выполняются во всех современных офтальмологических клиниках развитых стран, с применением уникальных технологий. Операции на сетчатке за рубежом постоянно совершенствуются, постоянно разрабатываются и внедряются в практику инновации, избавляющие от слепоты тысячи пациентов.
13 Ноября 2018
Почему сетчатка у человека не восстанавливается?
Биолог Алексей Ердяков о стволовых клетках сетчатки, клетках Мюллера и способностях к регенерации сетчатки у разных организмов
ПостНаука
Один из важных и интересных вопросов в области патофизиологии зрения – почему у некоторых животных способность к регенерации сетчатки после ее травмы сохранилась, а у человека такая способность отсутствует? Способность к регенерации сетчатки, то есть к ее полному функциональному восстановлению, давно изучается на различных видах животных, как-то: рыбки данио-рерио (zebrafish), шпорцевые лягушки и тритоны. После повреждения сетчатка у этих животных полностью восстанавливается и структурно, и функционально. А если у человека в сетчатке реализуется какой-то воспалительный процесс, он, как правило, заканчивается процессами глиоза, то есть пролиферации и фиброза глиальной ткани.
Один из важных и интересных вопросов в области патофизиологии зрения – почему у некоторых животных способность к регенерации сетчатки после ее травмы сохранилась, а у человека такая способность отсутствует? Способность к регенерации сетчатки, то есть к ее полному функциональному восстановлению, давно изучается на различных видах животных: рыбки данио рерио (zebrafish), шпорцевые лягушки и тритоны. После повреждения сетчатка у этих животных полностью восстанавливается и структурно, и функционально. А если у человека в сетчатке реализуется какой-то воспалительный процесс, он, как правило, заканчивается процессами глиоза, то есть пролиферации и фиброза глиальной ткани.
Не так давно были опубликованы результаты экспериментов, проводимых на мышах. Существует особый пронейрональный транскрипционный фактор, который у мышей, млекопитающих и человека в норме находится в молчащем состоянии, то есть неактивен. А у рыбок данио-рерио он находится в активном состоянии, при повреждении сетчатки он позволяет клеткам Мюллера дедифференцироваться, давать практически все возможные типы нейронов сетчатки: фоторецепторы, биполярные клетки, амакриновые клетки, которые обрабатывают первичную зрительную информацию на уровне сетчатки.
Этот пронейрональный транскрипционный фактор в клетках Мюллера удалось активировать, когда у мышей искусственно травмировали сетчатку, вносили повреждения. Клетки Мюллера подвергались дедифференциации и формировали пулы функционально активных нейронов в сетчатке. К сожалению, не получилось до конца восстановить сетчатку, и клетки Мюллера давали исключительно биполярные клетки. Никакие другие типы нейронов в результате своей дедифференцировки они больше не давали.
Возникает вопрос: что еще может влиять на регенераторный потенциал сетчатки у млекопитающих? Дело не только в одном транскрипционном факторе, хотя эти регуляторные механизмы на уровне клеток сейчас активно изучаются и многие исследователи этим занимаются. Нельзя говорить о том, что речь может идти о каких-то отдельных, индивидуальных транскрипционных факторах. Сетчатка – это сложно устроенная ткань, речь идет о большом количестве различных регуляторных факторах как на клеточном уровне, так и на тканевом уровне. Это очень большая, сложная система. Изучать ее нужно комплексно, не заострять свое внимание только на генетическом аппарате клетки и ее транскрипционных факторах.
Но, как и бывает в биологии, сведения накапливаются постепенно, поэтому единая концепция может вызревать позднее. Через 10–15 лет мы больше узнаем о факторах транскрипционных и о макрофакторах, которые регулируют воспалительные процессы уже на уровне ткани. Поймем, как это все совместно работает и как нам сделать так, чтобы заставить клетки Мюллера у человека регенерировать.
Почему в процессе эволюции так произошло, что некоторые организмы сохранили способность к регенерации сетчатки, а некоторые организмы утратили ее? В настоящее время рассматривают концепцию, заключающуюся в том, что существует два подхода к восстановлению сетчатки. Первая концепция – регенераторная, когда сетчатка полностью функционально восстанавливается из стволовых клеток и из аналогов стволовых клеток сетчатки. Это еще называется непролиферативный глиоз, то есть глиальные клетки, к которым клетки Мюллера тоже относятся, активируются на фоне развития местной воспалительной реакции. Но эта активация глиальных клеток приводит к дедифференциации клеток Мюллера и к тому, что сетчатка из этих клеток Мюллера может восстанавливаться.
А у человека и млекопитающих эволюция пошла по другому пути, и реализуется стратегия нейропротекции. Она хороша на коротких сроках, то есть тактически это хорошая стратегия, а вот стратегически – неудачная. Эта стратегия называется пролиферативным глиозом. С ее помощью реализуется замещение функциональных нейронов, которые осуществляют обработку зрительной информации в сетчатке, глиальной тканью – это и называется глиозом. То есть глия пролиферирует, и формируется глиозный рубец, который замещает область погибших нейронов. Эта стратегия реализуется не только для сетчатки, но для всей нервной ткани и головного мозга в том числе.
Помимо глиоза, над сетчаткой, под сетчаткой или внутри сетчатки образуются фиброзно-клеточные мембраны. Замещение происходит не только глиальными клетками, но и соединительной тканью. Если рассматривать регуляторные процессы, вырабатывается большое количество нейротрофических факторов. Это, например, мозговой нейротрофический фактор BDNF, фактор роста нервов NGF. Это различные нейротрофины – третий и четвертый. Благодаря воздействию нейротрофических факторов наши нейроны какое-то время могут просуществовать как можно дольше. Они обеспечивают сохранность нейронов на коротком промежутке времени. Однако в дальнейшем все заканчивается развитием тотального глиоза – замещением глиальными клетками и формированием соединительнотканных мембран. Такая стратегия реализуется у человека.
В дальнейшем понимание этих процессов и выстраивание более полноценной патофизиологической концепции того, что происходит на фоне развития внутриглазного воспаления, при травмах сетчатки и сопоставление этих данных с тем, что происходит у классических организмов, на которых изучают регенераторные возможности сетчатки, позволит прийти к тому, чтобы заставить наши потенциально стволовые клетки сетчатки регенерировать, а из них сетчатка восстанавливалась бы не только структурно, но и функционально.
Портал «Вечная молодость» http://vechnayamolodost.ru
Читать статьи по темам:
стволовые клетки зрение регенерация Ошибка в тексте? Выдели ее и нажми ctrl + enterназад