Содержание

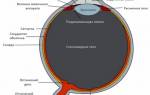
Мы привыкли ассоциировать зрение лишь с глазами. Однако помимо самих глазных яблок в процессе участвует зрительная кора головного мозга, которой мы фактически «видим», и нервные пути, которые соединяют глаза с мозгом. Практически на каждом этапе можно попытаться реализовать протезирование.
История создания зрительного протеза
Немецкий психолог Иоганн Пуркинье в 1823 году заинтересовался вопросами зрения и галлюцинаций, а также возможностью искусственной стимуляции зрительных образов. Принято считать, что именно он впервые описал зрительные вспышки — фосфены, которые он получил при проведении простого опыта c аккумулятором, пропуская через голову электрический ток и описывая свой визуальный опыт.
Спустя 130 лет, в 1956 году, австралийский ученый Дж. И. Тассикер запатентовал первый ретинальный имплант, который не давал какого-то полезного зрения, но показал, что можно искусственно вызывать зрительные сигналы.
Ретинальный имплант (имплант сетчатки) «вводит» визуальную информацию в сетчатку, электрически стимулируя выжившие нейроны сетчатки. Пока вызванные зрительные восприятия имели довольно низкое разрешение, но достаточное для распознавания простых объектов.
Но глазное протезирование долго тормозилось из-за технологических ограничений. Прошло очень много времени, прежде чем появились какие-то реальные разработки, которые смогли дать «полезное зрение», то есть зрение, которым человек мог бы воспользоваться. В 2019 году в мире насчитывалось около 50 активных проектов, фокусирующихся на протезировании зрения.
Первые ретинальные импланты
Пару лет назад на рынке было доступно три ретинальных импланта, которые прошли клинические испытания и были сертифицированы государственными регулирующими органами: европейским CE Mark и американским FDA.
- Second Sight Medical Products, США
- Pixium Vision, Франция
- Retina Implant AG, Германия

Бионические импланты — это целая система внешних и внутренних устройств.
IRIS II (Pixium Vision) и Argus II (Second Sight) имели внешние устройства (очки с видеокамерой и блок обработки видеосигнала). Слепой человек смотрит при помощи камеры, с нее картинка направляется в процессор, где изображение обрабатывается и распадается на 60 пикселей (для системы Argus II). Затем сигнал направляется через трансмиттер на электродную решетку, вживленную на сетчатке, и электрическим током стимулируются оставшиеся живые клетки.
В немецком импланте Alfa АMS (Retina Implant) нет внешних устройств, и человек видит своим собственным глазом. Имплант на 1600 электродов вживляется под сетчатку. Свет через глаз попадает на светочувствительные элементы и происходит стимуляция током. Питается имплант от подкожного магнитного коннектора.
Субретинальный имплантат Alpha AMS компании Retina Implant AG
Все три ретинальных импланта больше не производятся, так как появилось новое поколение кортикальных протезов (для стимуляции коры головного мозга, а не сетчатки глаза). Однако хотя проектов по фундаментальным разработкам по улучшению ретинальных имплантов еще много, ни один из них не прошел клинические испытания:
- Улучшенный имплант DRY AMD PRIMA компании Pixium с увеличением количества электродов для стимуляции большего количества клеток сетчатки проходит клинические испытания. Для участия в программе испытаний еще ищут пять кандидатов;
- Retina Implant AG закрыли производство;
- Second Sight проводят клинические испытания своего кортикального импланта, но в марте 2020 года компания уволила 80% сотрудников из эксплуатационно-производственного подразделения.
Тренды ретинальных имплантов: основные фундаментальные технологии
Ретинальные нанотрубки
Группа ученых из Китая (Shanghai Public Health Clinical Center) в 2018 году провела эксперимент на мышах, в ходе которого вместо не функционирующих фоторецепторов сетчатки предложила использовать нанотрубки. Преимущество этого проекта — маленький размер нанотрубок. Каждая из них может стимулировать только несколько клеток сетчатки.
Биопиксели
Группа ученых из Оксфорда стремится сделать протез максимально приближенным к естественной сетчатке. Биопиксели в проекте выполняют функцию, схожую с настоящими клетками. Они имеют оболочку из липидного слоя, в который встроены фоточувствительные белки. На них воздействуют кванты света и как в настоящих клетках изменяется электрический потенциал, возникает электрический сигнал.
Перовскитная искусственная сетчатка
Все предыдущие фундаментальные разработки направлены на стимулирование всех слоев живых клеток. При помощи технологии перовскитной искусственной сетчатки китайские ученые пытаются предоставить возможность не только получать световые ощущения, но и различать цвет за счет моделирования сигнала таким образом, чтобы он воспринимался мозгом как имеющий определенную цветность.
Фотогальваническая пленка Polyretina
В Polyretina используется маленькая пленка, покрытая слоем химического вещества, которое имеет свойство поглощать свет и конвертировать его в электрический сигнал. Пленка размещена на сферическом основании, чтобы можно было удобно разместить ее на глазном дне.
Фотогальванический имплант Polyretina
Субретинальное введение полупроводникового полимера
Итальянские ученые предлагают технологию введения полупроводникового полимерного раствора под сетчатку, при помощи которого свет фиксируется и трансформируется в электрические сигналы.
Российский опыт ретинального протезирования
В России в 2017 году при поддержке фондов «Со-единение» и «Искусство, Наука и Спорт» было приобретено и установлено два ретинальных импланта Argus II американской компании Second Sight. Это единственные операции по восстановлению зрения, которые были проведены в России за все время. Каждая операция вместе с реабилитацией стоила порядка 10 млн руб, а сама система имплантации для одного пациента — порядка $140 тыс. Все прошло успешно, и два полностью слепых жителя Челябинска — Григорий (не видел 20 лет) и Антонина (не видела 10 лет) — получили предметное зрение. Предметное зрение означает, что человек может видеть очертания предметов — дверь, окно, тарелку — без деталей. Читать и использовать смартфон они не могут. Оба пациента имели диагноз «пигментный ретинит» (куриная слепота).
На момент 2019 года в мире установлено около 350 имплантов, произведенных компанией Second Sight. Около 50 тысяч россиян нуждаются в подобном протезе сетчатки.
В России опытом в протезировании зрения может похвастаться лишь один проект — АНО Лаборатория «Сенсор-Тех».
«Трендом в фундаментальных разработках бионических протезов является стремление сделать их максимально безопасными, приближенными к биологическим тканям людей и с максимально возможным разрешением. Но настоящую революцию вызвали кортикальные импланты, и смысл в ретинальных имплантах пропал, так как они ставятся только при пигментном ретините и возрастной макулярной дегенерации при отсутствии ряда противопоказаний. Кортикальные же импланты значительно расширяют горизонт показаний и позволяют восстанавливать полезное зрение даже людям, вовсе лишенным глаз», — рассказал Андрей Демчинский, к.м.н., руководитель медицинских проектов АНО Лаборатория «Сенсор-Тех».
Кортикальные системы имплантации
Кортикальные протезы — это подгруппа визуальных нейропротезов, способных вызывать зрительные восприятия у слепых людей посредством прямой электрической стимуляции затылочной коры мозга, которая отвечает за распознавание изображений. Этот подход может быть единственным доступным лечением слепоты, вызванной глаукомой, терминальной стадией пигментного ретинита, атрофией зрительного нерва, травмой сетчатки, зрительных нервов и т.п. За последние пять лет ученые решили задачу создания такого внутрикортикального визуального нейропротеза, с помощью которого можно было бы восстановить ограниченное, но полезное зрение.
В 1968 году Г.С. Бридли и В.С. Левин провели первую операцию по установке кортикальных имплантов. Первый имплант состоял из шапочки с коннекторами (устанавливали на череп под кожу) и отдельной дуги с электродами (устанавливали под череп), которые стимулировали кору головного мозга. Эксперимент был проведен на двух добровольцах для оценки возможности получения полезного зрения. Позднее импланты были извлечены. Технология кортикальных имплантов была заморожена по причине провоцирования приступов эпилепсии при стимуляции большего количества клеток мозга.
Первый кортикальный имплант
Кортикальный имплант Orion
Спустя 45 лет американский лидер разработки ретинальных имплантов Second Sight создал кортикальную протезную систему ORION. В конце 2017 года Second Sight получили разрешение от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) на проведение клинических испытаний. До апреля 2018 года было установлено шесть устройств. По результатам испытаний оказалось, что все пациенты ощущали зрительные стимулы, a у трех пациентов результаты были схожи с ретинальным имплантом Argus II и дали полезное предметное зрение. Клинические испытания будут проходить до июня 2023 года. Обязательным условием установки импланта является наличие у пациента зрительного опыта, то есть он может использоваться только для людей со сформированной зрительной корой, которые родились зрячими и потеряли зрение.
Система кортикальной имплантации Orion компании Second Sight
Кортикальный нейропротез CORTIVIS
Испанские ученые разработали кортикальный имплант под названием CORVITIS. Протез состоит из нескольких компонентов. Одна или две камеры обеспечивают получение изображения, которое затем обрабатывается биопроцессором, чтобы преобразовать визуальный образ в электрические сигналы. На втором этапе информация сводится в серию изображений и передается по радиочастотной связи на имплантированное устройство. Этот радиочастотный блок обеспечивает беспроводную передачу питания и данных во внутреннюю систему. Имплантированный электронный блок декодирует сигналы, определяет и контролирует форму напряжения и амплитуду формы волны, которая будет подаваться на соответствующие электроды. Клинические испытания на пяти пациентах завершатся в мае 2023 года.
Кортикальный имплант CORVITIS
Интракортикальный зрительный протез (WFMA)
Американские ученые разработали технологию многоканальной внутрикортикальной стимуляции с помощью беспроводных массивов металлических микроэлектродов и создали беспроводную плавающую микроэлектродную решетку (WFMA).
Система протеза состоит из группы миниатюрных беспроводных имплантируемых решеток-стимуляторов, которые могут передавать информацию об изображении, снятом на встроенную в очки видеокамеру, непосредственно в мозг человека. Каждая решетка получает питание и цифровые команды по беспроводной связи, так что никакие провода или разъемы не пересекают кожу головы. Посылая команды в WFMA, изображения с камеры передаются непосредственно в мозг, создавая грубое предметное визуальное восприятие изображения. Хотя восприятие не будет похоже на нормальное зрение, с его помощью человек может вести самостоятельную деятельность. Система ICVP получила одобрение FDA для проведения клинических испытаний.
Интракортикальный зрительный протез (WFMA)
Кортикальный протез NESTOR
Голландские ученые также разработали схожую технологию системы протезирования. Принцип функционирования протеза такой же, как в проектах выше. Камера отправляет сигнал на имплант, который состоит из тысяч электродов и смарт-чипа. С помощью процессора зрительное восприятие можно контролировать и регулировать.
«Хотя полное восстановление зрения пока кажется невозможным, кортикальные системы создают по-настоящему значимые визуальные восприятия, при помощи которых слепые люди могут распознавать, локализировать и брать предметы, а также ориентироваться в незнакомой среде. Результат — в существенном повышении уровня жизни слепых и слабовидящих. Такие вспомогательные устройства уже позволили тысячам глухих пациентов слышать звуки и приобретать языковые способности, и такая же надежда существует в области визуальной реабилитации», — обнадежил Андрей Демчинский.
Обновлено 14.08.2020Установка “внутриглазных очков”, позволяющих справиться с близорукостью 25 диоптрий и более, вживляемые линзы, благодаря которым забудете о сильном астигматизме, удаление опухоли глаза, сохраняющее и глаз, и зрение… Эти и другие уникальные вмешательства выполняются в петербургском филиале Национального медицинского исследовательского центра “Микрохирургия глаза” имени С. Н. Федорова. Сюда стремятся попасть на лечение и россияне, и жители стран, располагающих высотехнологичной медициной. Сегодня Эрнест Бойко, директор филиала, в прошлом военный врач-офтальмолог, – гость “РГ”. Эрнест Бойко: Будущее за технологиями, позволяющими “вырастить” глаз и его части на основе собственных клеток пациента. Фото: Сергей Николаев/РГ
Не можем обойти тему коронавируса. Как пандемия сказалась на работе клиники?
Эрнест Бойко: По просьбе комитета по здравоохранению города мы, клиника плановой госпитализации, стали принимать больных по скорой. Потому что многие больницы, имеющие офтальмологические отделения, перепрофилировали под прием пациентов с COVID-19. В сутки принимаем до 40 экстренных больных с отслойкой сетчатки, после травм и с другими проблемами. Здесь пригодился и опыт военной офтальмологии, и опыт плановых высоких технологий, от сочетания которых выигрывает пациент.
Одна из самых популярных операций – замена искусственного хрусталика. Святослав Федоров разработал искусственный хрусталик и стал делать операции в начале 1960-х годов. Каковы сейчас возможности лечения катаракты?
Эрнест Бойко: Технологии другие: риски снизились до долей процента, а операции стали давать очень комфортное зрение. Что касается искусственных хрусталиков, то есть новейшие модели – бифокальные, трифокальные и другие, с помощью которых можно корректировать различные параметры глаза и которые позволяют достичь отличного зрения в сложных случаях.
Оперируем с помощью полуроботических систем. Параметры рассчитываются с помощью интеллектуальной компьютерной системы.
Когда лучше оперировать катаракту? Ждать ли “созревания”?
Эрнест Бойко: Каждый пациент решает сам. Кто-то говорит: “Я еще могу читать, я боюсь операции, я подожду”. А для кого-то аналогичное состояние – крайний дискомфорт, и тогда лучше ее сделать раньше. Показание для неотложного вмешательства: “набухание” катаракты и резкое ухудшение зрения.
Глаукома – приговор судьбы?
Эрнест Бойко: Процесс реально притормозить. У нас сейчас для этого используются щадящие хирургические методики. Что касается амбулаторного лечения: если при длительном нахождении “на каплях” глазное давление не снижается до показателей 18-19 миллиметров ртутного столба, ситуация может стать опасной для глаз. Оперированная глаукома всегда протекает лучше неоперированной! Как пример – пациент с тяжелой формой глаукомы, который в течение 29 лет перенес много операций, но он видит!
В “Микрохирургии глаза” в 1990-х впервые в стране стали делать операции по корректировке близорукости с помощью насечек на роговице. Теперь предлагается эксимерный лазер?
Эрнест Бойко: Он в какой-то степени вчерашний день. У нас есть самая мощная в стране линейка фемтосекундных лазеров, с помощью которых можно достичь фантастических результатов. Если частота отдаленных последствий у эксимерного лазера около одного процента, то при фемто не более 0,5 процента. Точность операции – до доли микрона! Это принципиально новые возможности тканесберегающей рефракционной хирургии! И если раньше конечный результат был плюс-минус 0,5 диоптрии, то теперь он 0,25! Лазер работает внутри глаза, “выкраивая” крошечную часть роговицы – в виде чечевицы. Хирург вынимает кусочек через разрез, который напоминает смайлик-улыбку, операцию называют “Смайл”.
Филиал – передовой в плане внедрения новинок. Расскажите о них.
Эрнест Бойко: В одну из поездок в Санкт-Петербург Святослав Федоров поделился мечтой о том, чтобы очки не носить снаружи, а имплантировать внутрь глаза, и в этом году специалисты филиала широко начали применять технологию имплантации “внутриглазных очков”. На хрусталик пациента ставится гелеобразный хрусталик. С его помощью исправляется зрение – как вблизи, так и вдаль. Это мечта Федорова, ставшая явью. Пример: пациентка с близорукостью 25 диоптрий, которая не корректировалась очками. С “внутриглазными очками” она сразу после операции стала отлично видеть. У нее слезы на глазах от счастья: она читает девять строк таблицы!
Высокоточная хирургия макулярных разрывов сетчатки (макула – желтое пятно, самый центр сетчатки). Операции проходят с помощью 4D-технологий. Это четырехмерная хирургия. Объясню проще: вы смотрите на стену, видите стену в трехмерном изображении. В четырехмерном – слои предыдущих обоев, кирпич.
Гигантский рывок в офтальмоонкологии. При новообразованиях глаза его обычно удаляют, и это большая психологическая травма для пациента. У нас разработана методика, позволяющая сохранить и глаз, и зрение. С помощью радиации и лазеров, которые воздействуют на опухоль, мы ее облучаем и подавляем. Далее по необходимости проводим эндорезекцию (удаление).
Проблема нашего времени – возрастная макулярная дегенерация. Макула тонка и с возрастом начинает страдать от недостатка кислорода. Организм пытается спасти ситуацию, допуская к макуле новые сосуды. Но они неполноценны и дают отек: человек теряет центральное зрение. Он не ослепнет, но читать не сможет. Мы начали выполнять уникальные операции: из кусочка глазного пигментного эпителия пациента делаем “заплатку” на тонкую макулу, восстанавливая зрение.
Можно ли сделать операции бесплатно?
Эрнест Бойко: Да, но зависит от вида операций. Операции по коррекции близорукости не входят в госпрограмму. А пересадка роговицы, лечение глаукомы, катаракты, онкологии, заболеваний сетчатки, например, входят. Нужно лишь оформить соответствующее направление. Приехать к нам можно из любого региона, а не только из Петербурга и СЗФО. Но если пациент хочет и хрусталик заменить, и одномоментно поставить внутрь глаза торические линзы, позволяющие исправить сильный астигматизм, то бесплатно не получится. Торические линзы в госпрограмму пока не входят. Это же касается и мультифокальных хрусталиков, позволяющих почти всегда избавиться от очков.
Пациентка с близорукостью 25 диоптрий сразу после имплантации “внутриглазных очков” стала отлично видеть
Есть ли очереди на лечение катаракты по ОМС?
Эрнест Бойко: В нашем учреждении – около двух лет. Но в тяжелых случаях, когда пациент из-за падения зрения не может себя обслуживать, берем гораздо быстрее. Мы значительно увеличили число операций за счет отказа от круглосуточного стационара. Поясню: государственные тарифы позволяют, например, на одну и ту же сумму либо прооперировать трех пациентов с госпитализацией в стационар на сутки, либо прооперировать четырех пациентов в амбулаторном режиме. Мы выбираем второй вариант. Также весь спектр операций можно выполнить быстро, – на хозрасчетной основе.
Как узнать, все ли в порядке с глазами?
Эрнест Бойко: Пройти обследование у офтальмолога, желательно с применением современного оборудования.
“Микрохирургия глаза” ведет активную образовательную деятельность. Вы первыми в стране открыли “ВетЛаб”, в которой учатся будущие хирурги-офтальмологи. Как обстоят дела сейчас?
Эрнест Бойко: За 20 лет подготовлено более двух тысяч специалистов из РФ, СНГ, других стран. Врачи учатся как на хирургическом симуляторе, позволяющем отточить методику высочайшей точности, так и делают операции на глазах лабораторных животных. У нас также обучаются преподаватели вузов (бесплатно, по квотам).
Операции настолько уникальны, что лечиться к вам приезжают из стран, где медицина высокого уровня. Будете развивать медицинский туризм?
Эрнест Бойко: Да. Рассчитываем на упрощенный порядок выдачи визы и безвизовое кратковременное пребывание. Обследование пациента и операция занимают пару часов, после которых турист может любоваться красотами Петербурга “новым зрением”.
Философский вопрос оперирующему офтальмологу: что такое глаза?
Эрнест Бойко: Нравится определение: глаз – это мозг, вынесенный на периферию. Это сложнейшее устройство, через которое человек получает 90 процентов информации, и я согласен, что глаза – зеркало души.
Что мы можем делать для сохранения зрения?
Эрнест Бойко: Вести здоровый образ жизни. Правильно питаться (включите в меню продукты, богатые флавоноидами и лютеином: морковь, томаты, перец красный и желтый, чернику). Ограничьте время пользования гаджетами. После одного-полутора часов работы за компьютером делайте 15-минутный перерыв (встаньте у окна и смотрите вдаль, сделайте гимнастику).
Ваша мечта?
Эрнест Бойко: Победить непобедимое. Сейчас, если пострадал зрительный нерв, помочь нельзя. Не можем “оживить” умершие ткани, например сетчатку. Будущее за технологиями, позволяющими “вырастить” глаз и его части на основе собственных клеток пациента.
Статистика
Петербургский филиал НМИЦ “Микрохирургия глаза” выполняет до 27 тысяч операций в год, из них до девяти тыcяч – при катаракте, до четырех тысяч – при глаукоме, две тысячи – на стекловидном теле и сетчатке, более пяти тысяч – фемтолазерная коррекция и другие.
Актуально
С праздником!
Офтальмологи поздравляют с Новым годом и Рождеством.
“Уходит сложный високосный год, который испытал и закалил нас, обогатил новым опытом и впечатлениями, – говорит Эрнест Бойко. – Пусть наступающий год будет щедрым на успехи, хорошие события, развитие и профессиональные победы, принесет счастливое время новых возможностей и достижений! Сердечно желаю вам и вашим близким прекрасного зрения, крепкого здоровья, уюта и тепла в вашем доме!”
Фото: Архив петербургского филиала НМИЦ “Микрохирургия глаза” имени С. Н. Федорова В регионах Филиалы РГ Северо-Запад СЗФО Санкт-Петербург
Ученые МФТИ в сотрудничестве с исследователями Гарварда вырастили клетки сетчатки, которые способны врастать в глаза. Это первая в мире успешная попытка трансплантации ганглионарных клеток (нейроны сетчатки, которые разрушаются при глаукоме), полученных из стволовых клеток в лабораторных условиях. Далее выращенные клетки нужно будет трансплантировать в сетчатку. Ученые проверили технологию на мышах и удостоверились в успешном встраивании клеток и их выживании на протяжении года. В дальнейшем исследователи планируют создать специализированные банки клеток, которые позволят индивидуально подбирать терапию для каждого пациента.
Операция «Трансплантация»
Первую в мире успешную попытку выращивания и трансплантации ганглионарных клеток сетчатки из стволовых произвели ученые лаборатории геномной инженерии МФТИ в сотрудничестве с исследователями Гарвардской медицинской школы. Ганглионарные клетки ответственны за передачу зрительной информации, и именно они повреждаются при глаукоме. Ученым удалось не только вырастить нейроны (ганглионары считаются специализированными нейронами), но и трансплантировать их в глаза мышей, добившись правильного врастания искусственной ткани сетчатки. Как известно, без лечения развитие глаукомы может привести к необратимому повреждению части зрительного нерва и, как следствие, потери части визуального поля. Прогрессируя в течение долгого времени, эта болезнь может привести и к полной слепоте.
В поле зрения: ученые открыли ген наследственной слепоты Болезнь вызывает мутация, из-за которой перестает вырабатываться важный белок
Клетки сетчатки были выращены в специальных органоидах, ткань формировалась в пробирке, рассказал «Известиям» младший научный сотрудник лаборатории геномной инженерии МФТИ Евгений Кегелес. Потом эти клетки пересадили мышам, которые были распределены в несколько групп.
— Были мыши с моделью глаукомы, мыши с повышенным внутриглазным давлением и те, у которых были удалены собственные ганглионары, — отметил Евгений Кегелес. — Были также новорожденные мыши: мы проверяли гипотезу более успешной приживаемости молодых ганглионарных клеток в формирующейся сетчатке. В результате оказалось, что клетки встроились и прорастили аксоны, которые позволят связать глаз с мозгом. Улучшенная выживаемость клеток у новорожденных мышей дает нам перспективное направление для поиска наилучшего микроокружения.
По словам Евгения Кегелеса, эти клетки успешно просуществовали внутри сетчатки 12 месяцев, что является серьезным сроком для такого исследования. Ученым удалось убедиться, что они получают зрительные сигналы, однако то, что клетки передают сигналы в мозг, со стопроцентной уверенностью утверждать пока нельзя.
— Мы точно знаем, что выращенные клетки встраиваются куда надо, протягивают аксоны в мозг, но их функциональность оценить пока невозможно, — объяснил Евгений Кегелес. — Это связано с тем, что до сих пор нам не удалось вырастить большое количество клеток. Это вопрос ближайших лет.
По его словам, исследователям нужен год, чтобы они смогли оценить функциональность клеток на мышиных моделях. В течение этого времени можно будет получить доказательство, что клетки не просто правильно встроены в структуру глаза, а они именно «видят».
Клеточный банк
Сейчас мышиные клетки сетчатки удается вырастить примерно за 21 день. В случае человека это будет от 50 до 100 дней, говорят ученые МФТИ.
Однако, скорее всего, человеку с глаукомой, готовящемуся к трансплантации, не нужно будет выращивать ткань сетчатки из собственных стволовых клеток. Так как глаз является иммунопривилегированным органом, где отторжения редки, возможно создать банк клеток для таких пациентов. Там будут размещены или выращенные клетки сетчатки от универсального донора, или из индуцированных плюрипотентных стволовых клеток. Это значит, что можно будет заранее вырастить клетки, заморозить их и, когда пациент с глаукомой обратится за помощью, подобрать для него наилучший клеточный вариант для трансплантации.
Земля не плоская: вернуть объемное зрение помогут компьютерные очки Разработанный российскими учеными прибор исправит серьезную патологию за несколько месяцев в домашних условиях
Впоследствии эту технологию можно будет применять и для лечения других заболеваний глаз, например дистрофии сетчатки. Однако выращивать придется другие клетки.
— Нобелевскую премию за индуцированные плюрипотентные стволовые клетки дали почти 10 лет назад, в 2012 году, — отметил руководитель лаборатории геномной инженерии Павел Волчков. — Так называемый хайп, когда буквально все научные коллективы считали своим долгом заниматься этой тематикой, давно угас. Сейчас настало время не просто слов, а реальных технологий на основе iPS (искусственные плюрипотентные стволовые клетки человека. — «Известия»). И именно к таким технологиям относится исследование по трансплантации ганглионаров сетчатки. Это возможность показать, что стволовые клетки реально можно применить на практике, с их помощью можно что-то исправить. Хотя эта работа еще не доведена до клиники, но она уже в нескольких шагах от реальной пересадки с целью лечения глаукомы.
Учитывая большой опыт экспериментальных работ мировых ученых и активное изучение вопроса заместительной клеточной терапии в офтальмологии, в дальнейшем метод может привести к прорыву в диагностике и лечении глаукомы, считает заведующая отделением офтальмологии ФГБУ НМИЦО ФМБА России, действительный член Европейского общества катарактальных и рефракционных хирургов (ESCRS), член Российского общества офтальмологов Ника Тахчиди.
Слепой метод: что помогает незрячим ориентироваться в телефоне и мире Прототипов сотни, реально доступных устройств — единицы
— В ряде зарубежных работ показано, что введенные клетки встраиваются в сетчатку и частично дифференцируются в клетки сетчатки. В настоящее время описаны и обсуждаются два основных механизма действия клеток in vivo и in vitro. Замещающая терапия — когда клетки, образующиеся в результате дифференцировки введенных стволовых клеток, «включаются» в восстанавливаемую ткань. «Эффект стороннего наблюдателя» — когда вводимые стволовые клетки оказывают противовоспалительное, трофическое или иммуномодулирующее действие на восстанавливаемую ткань. Однако, несмотря на прорыв в изучении морфофунциональных свойств стволовых клеток, обеспечить гарантированное послойное замещение культивированными клетками поврежденных участков сетчатки при использовании практикуемых методов введения на сегодняшний день невозможно, что и подтверждается рядом экспериментальных работ, — сказала Ника Тахчиди.
Впрочем, многие ученые в мире сейчас работают в этом направлении, пытаясь создать клеточную терапию лечения атрофии зрительного нерва, дистрофии сетчатки и глаукомы, отметила заведующая отделением офтальмологии клинико-диагностического центра «Медси», врач-офтальмолог Ирина Евсегнеева.
— Но никаких данных на сегодняшний день о том, что пересаженные клетки передают изображение, нет. Любая идея, как это сделать, заслуживает внимания, — сказала она.
По оценке ученых МФТИ, на доведение технологии до применения в лечебной практике уйдет примерно 10 лет.
Читайте также Подготовка пациента перед витреоретинальной операцией (по поводу заболеваний сетчатки глаза) и памятка пациента после проведения операции.
ПАМЯТКА ПАЦИЕНТУ
(витреоретинальная операция) Уважаемый пациент!
Вам предстоит витреоретинальная операция. Операция проводится под местным, внутривенным или общим обезболиванием. Длительность операции от 30 до 120 минут. Операция предполагает особый предоперационный и послеоперационный режим.
Перед операцией Вам необходимо:
-
пройти консультацию врача-анестезиолога с готовыми результатами анализов;
-
капли начинать закапывать за сутки до операции:
Ципрофлоксацин – по 2 капли 4 раза в день
Неванак (Индоколлир) – по 2 капли 3 раза в день
-
в день операции не пользоваться средствами косметики, макияжа и духами;
-
накануне операции тщательно помыть голову и лицо;
-
все лекарственные препараты, которые Вы принимаете регулярно, продолжайте принимать в обычном режиме;
-
утром в день операции можно легкий завтрак. Если планируется проведение наркоза, есть и пить нельзя за 4 часа до операции;
-
в день операции при себе иметь: паспорт, договор на оказание медицинских услуг, солнцезащитные очки и чистую сменную обувь (тапочки).
|
Госпитальный хирургический комплекс (срок годности 1 месяц) 1. Анализ крови клинический, СОЭ 2. Коагулограмма (АЧТВ, протромбин по Квику, МНО, фибриноген) 3. Биохимия крови: креатинин, мочевина, белок, общий билирубин, АлТ, АсТ, глюкоза; 4. Анализ крови на ВИЧ, RW, HBS-антиген, HCV – антиген (срок годности 3 месяца); 5. Анализ мочи клинический; 6. Электрокардиография с заключением; 7. Флюорография (срок годности 12 месяцев); 8. Заключение врачей-специалистов (стоматолога, отоларинголога, терапевта) об отсутствии противопоказаний к операции; 9. При наличии хронических заболеваний – заключение специалистов, у которых пациент наблюдается. При сахарном диабете – консультация эндокринолога обязательна. |
После операции:
Вам провели операцию на глазу. В течение 1 часа после операции Вы будете находиться под наблюдением медицинского персонала клиники.
Обязательно наличие сопровождающих лиц для транспортировки пациента после операции к месту проживания. Для транспортировки предпочтительно использовать частный автотранспорт.
На следующий день после операции Вам необходимо явиться на обязательный послеоперационный осмотр. В течение 10-14 дней после операции Вам будут необходимы периодические послеоперационные осмотры по назначению лечащего врача.
Первые 14 дней:
- пользуйтесь только специальными каплями по назначению врача.
Первый месяц:
-
запрещается заниматься тяжелой физической работой, поднимать тяжести, передвигать мебель;
-
не рекомендовано посещать парную и сауну;
-
пища может быть обычной;
-
можно смотреть телевизор, ходить в кино, театр и т.п., не забывая закапать капли в глаз;
-
общение с большим количеством людей в раннем послеоперационном периоде желательно ограничить (особенно в периоды эпидемий острых респираторных заболеваний).
Через 1 месяц после операции перечисленные ограничения отменяются, и Вы сможете вернуться к своему обычному образу жизни.
Врач-офтальмолог может дать Вам дополнительные рекомендации и назначить время осмотра. В случаях, если потребуется срочная консультация, помощь (травма, внезапное снижение зрения, воспаление глаза и т.п.), Вам необходимо срочно обратиться к лечащему врачу.
Все обследования и консультации в клинике осуществляются по предварительной записи.
Напоминаем Вам, в течение первого месяца после операции 3 осмотра проводятся без оплаты. Обращения в сроки от 1 до 6-ти месяцев оплачиваются со скидкой, после 6-ти месяцев (со дня операции) за полную стоимость.
Схема закапывания капель после операции
Капли можно закапывать самостоятельно или это могут делать родственники. Вымыв руки с мылом, оттяните вниз нижнее веко оперированного глаза, в образовавшуюся между веком и глазом ложбинку капните 1 каплю лекарства (не дотрагиваться до глаза пипеткой, не прикасаться флаконом к векам и ресницам!). При этом смотреть лучше вверх. Удобно закапывать лекарства, лежа на спине. Перерыв между закапыванием разных лекарств не менее 5-10 минут. Сначала закапывают рекомендованные лечащим врачом глазные капли, затем мазь. Ночью капать капли не нужно.
Ципрофлоксацин – 2 капли 4 раза в день – 2 недели
Тобрадекс (Тобразон) – 2 капли 4 раза в день – 3 недели
Неванак (Индоколлир) – 2 капли 3 раза в день – 1 месяц
Мазь Флоксал – 3 раза в день – 5-7 дней
Схема закапывания может быть назначена врачом индивидуально.
В случаях, когда требуется срочная консультация, помощь (внезапное снижение зрения, воспаление глаза и т.п.) Вам нужно срочно обратиться в клинику к Вашему лечащему врачу. В рабочее время Вы можете позвонить по телефону +7-(495)123-31-12. В нерабочее время можно позвонить хирургу:
|
Для Вашего удобства предлагаем схему закапывания капель после операции по часам |
||||
|
препаратчасы |
9:00 |
13:00 |
18:00 |
22:00 |
|
Ципрофлоксацин – 2 недели |
х |
х |
х |
х |
|
Тобрадекс (Тобразон) – 3 недели |
х |
х |
х |
х |
|
Неванак (Индоколлир) – 1 месяц |
х |
х |
х |
|
|
Мазь Флоксал – 5-7 дней |
х |
х |
х |
Желаем Вам скорейшего выздоровления!