Содержание
- Содержание статьи:
- Причины заболевания
- Симптомы неврита зрительного нерва
- Классификация и стадии развития болезни
- Осложнения неврита зрительного нерва
- Диагностика заболевания
- Лечение неврита зрительного нерва
- Профилактика заболевания
- История создания зрительного протеза
- Первые ретинальные импланты
- Тренды ретинальных имплантов: основные фундаментальные технологии
- Российский опыт ретинального протезирования
- Кортикальные системы имплантации
Содержание статьи:
Неврит зрительного (глазного) нерва, оптический неврит, – первичный воспалительный процесс, причинами которого являются различные факторы. Частота возникновения в расчете на 100 тыс. населения – от 1 до 5 случаев. Среди всех заболеваний глаз поражение зрительного нерва фиксируется в 3,2 % случаев. Патология отличается высокой частотой возникновения необратимых последствий (снижение зрения, слепота) и инвалидизации – по данным разных исследований они наступают в 20-28 % случаев.
Причины заболевания
Чаще всего неврит зрительного нерва развивается при рассеянном склерозе и является его первым проявлением. Основа воспалительного процесса в этом случае – демиелинизация, или разрушение миелиновой оболочки нерва. Поражение зрительного нерва провоцируют и другие аутоиммунные патологии: системная красная волчанка, синдром Шегрена.
К демиелинизации и, как следствие, невриту зрительного нерва также приводят заболевания, связанные с сывороточными иммуноглобулинами G к миелин-олигодендроцитарному гликопротеину (MOG-IgG), в частности, острый рассеянный энцефаломиелит.
Аксоны и нейроны глазного нерва разрушаются не только в результате демиелинизирующих процессов, но и на фоне других болезней. К ним относятся:
- воспаления глазного яблока и/или орбиты;
- воспалительные заболевания головного мозга;
- инфекционные процессы в носоглотке;
- саркоидоз, гранулематоз;
- острое нарушение мозгового кровообращения;
- эндокринные патологии – тиреотоксикоз, сахарный диабет;
- специфические инфекции – туберкулез, сифилис, грипп.
Неврит зрительного нерва может быть следствием травмы глаза, черепно-мозговой травмы, токсического поражения – в большинстве случаев это отравление метиловым спиртом, свинцом, иногда – глистные инвазии. Может провоцироваться осложненной беременностью.
Симптомы неврита зрительного нерва
Симптоматика различается в зависимости от вида заболевания: интрабульбарный (папиллит) или ретробульбарный неврит.
Папиллит (внутриглазной, ретробульбарный неврит)
Характеризуется острым началом с быстрым ухудшением остроты зрения – от 1-2 часов до 1-2 суток. В некоторых случаях возникают умеренная головная боль и боль при движении глаз. При частичном поражении острота зрения может сохраняться, но появляются скотомы – участки частичного или полного выпадения поля зрения, которые могут быть центральными и парацентральными, округлыми или аркоподобными. Возможно сужение границ поля зрения, снижение темновой адаптации и цветового восприятия. Чаще всего симптомы ухудшения зрения исчезают через 7-10 дней, через 2-3 недели (иногда – до 5 недель) зрение восстанавливается. Без лечения либо при тяжелом течении неврита возможна атрофия зрительного нерва с полной потерей зрения.
Ретробульбарный неврит
Протекает в острой или хронической форме. Острая форма чаще характерна для одностороннего поражения, хроническая – для двустороннего.
Общие симптомы:
- болезненность при движении глазными яблоками и надавливании на глаз;
- нарушения цветового зрения – снижение чувствительности глаза к цветам, оттенки быстро тускнеют;
- падение остроты зрения до полной невозможности различать предметы;
- появление скотом.
В зависимости от формы ретробульбарного неврита симптомы могут различаться. Для аксиального неврита характерно сочетание центральной скотомы с частичными выпадениями полей зрения и возникновением в поле зрения периферических дефектов. При периферической форме поле зрения имеет сужается по всему периметру – имеет концентрический характер. Трансверсальная форма отличается значительным снижением зрения, вплоть до слепоты, скотомами, сливающимися с периферическими выпадениями полей зрения.
Классификация и стадии развития болезни
В зависимости от зоны поражения:
- Интрабульбарный (внутриглазной) неврит, оптический папиллит. Это воспаление внутриглазной части (диска) зрительного нерва. Чаще развивается у детей.
- Ретробульбарный неврит. Повреждение отдела нерва, лежащего между глазным яблоком и перекрестом зрительных нервов. Формы ретробульбарного неврита :
- аксиальная – в патологический процесс вовлечен пучок аксонов, проходящих в зрительном нерве;
- периферическая – воспаление охватывает оболочки нерва и распространяется вглубь нервного ствола с образованием большого количества экссудата под оболочками;
- трансверсальная – процесс затрагивает все слои зрительного нерва.
По этиологии поражения:
- инфекционный:
- параинфекционный (поствакцинальный, после перенесенных ОРВИ);
- демиелинизирующий;
- ишемический;
- токсический;
- аутоиммунный.
По остроте течения:
- острый;
- хронический.
По распространенности поражения:
- мононеврит – воспаление одного нерва (подавляющее большинство случаев);
- полиневрит – вовлечение в процесс обоих зрительных нервов (менее 1 % случаев).
Осложнения неврита зрительного нерва
Переход процесса в хроническую форму, сопровождающуюся частыми рецидивами и нарушением зрения. Основное и наиболее опасное осложнение неврита глазного нерва – его атрофия с деструкцией миелиновой оболочки и полной потерей зрения.
Диагностика заболевания
Как правило, пациенты, у которых появились первые симптомы неврита зрительного нерва, обращаются к офтальмологу. Заболевание считается междисциплинарной патологией, в его лечении обязательно принимают участие окулист либо невропатолог. Если неврит развивается на фоне других патологий, необходимо уточнять диагноз и проводить специфическую терапию первичных болезней . Тогда к лечению подключаются соответствующие специалисты – иммунолог, оториноларинголог, инфекционист, фтизиатр.
Первым этапом в диагностике неврита зрительного нерва являются сбор анамнеза, внешний осмотр пациента, пальпация. Во время сбора анамнеза врач уточнит наличие сопутствующих патологий, время начала заболевания, какие жалобы предъявляет больной (боль, снижение остроты зрения, изменение цветоощущения, появление «слепых» пятен), как быстро развивались симптомы и насколько они выражены, поражен один глаз или оба.
Внешний осмотр и пальпация зачастую могут не принести дополнительных данных. Боль, смещение вперед глазного яблока, ограничение его движений могут возникать при ретробульбарном неврите, но не являются обязательными.
Далее врач переходит к офтальмологическому осмотру. Он включает в себя:
- определение остроты зрения;
- исследование цветоощущения проводится по полихроматическим таблицам Рабкина;
- исследование реакции зрачка на свет;
- измерение внутриглазного давления, которое может быть симптомом глаукомы и других заболеваний, провоцирующих развитие неврита;
- биомикроскопия – осмотр переднего отрезка глаза для исключения его патологии;
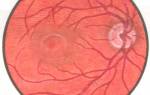
- офтальмоскопия (осмотр глазного дна) после закапывания капель, расширяющих зрачок;
- компьютерное исследование полей зрения по 120 точкам;
- исследование полей зрения методом кинетической периметрии.
Для уточнения диагноза используются следующие методы:
- электрофизиологическая диагностика – исследование порога электрической чувствительности сетчатки и зрительных вызванных потенциалов;
- ультразвуковое исследование глаз, МРТ орбиты глаза и головного мозга;
- когерентная томография зрительного нерва;
- флюоресцентная ангиография сетчатки.
Лабораторная диагностика:
- общий анализ крови;
- кровь на ВИЧ, сифилис, ревматоидный фактор;
- посев крови на стерильность;
- ПЦР-исследования;
- гистологический, иммунохимический анализ.
При наличии у больного сопутствующих заболеваний, ему назначают консультации узких специалистов.
Лечение неврита зрительного нерва
Лечение обязательно проводится в стационарных условиях, начинать его следует как можно раньше, во избежание перехода болезни в хроническую форму и развития осложнений . Больным с невритом зрительного нерва показана диета № 15 – общий стол, при отсутствии показаний к другим видам лечебных диет.
Основой лечения является этиотропная терапия, направленная на устранение первичного заболевания, послужившего причиной зрительного неврита. До выяснения этиологии болезни применяются средства, призванные уменьшить симптомы воспаления, убрать отечность, аллергические проявления, улучшить обмен веществ. Для этого применяются:
- глюкокортикостероидные препараты, при их непереносимости – нестероидные противовоспалительные средства (назначаются в редких случаях);
- антибактериальная или противовирусная терапия;
- противогрибковые средства с целью предотвращения грибковой инфекции вследствие длительного курса антибиотиков;
- дезинтоксикационная терапия – внутривенное капельное введение солевых растворов;
- антигистаминные препараты;
- диуретики;
- средства, улучшающие микроциркуляцию;
- нейропротекторы;
- витамины.
В дополнение к медикаментозным препаратам в лечении неврита зрительного нерва может использоваться физиотерапия.
При папиллите, а также инфекционно-токсической этиологии заболевания прогноз более благоприятный, чем при других видах невритов зрительного нерва, – в 75-90 % случаев при правильном лечении зрение восстанавливается полностью. При поражении глазного нерва вследствие аутоиммунных, демиелинизирующих заболеваний, коллагенозов, саркоидозов, специфических инфекций нередко возникают рецидивы, неполное восстановление зрения, возможна атрофия нерва .
Профилактика заболевания
Для профилактики неврита зрительного нерва рекомендуется отказаться от вредных привычек, своевременно лечить инфекционные заболевания, избегать травм глаза и головы, посещать профильных врачей при наличии хронических патологий.
Источники статьи:
- Ретробульбарный неврит зрительного нерва. Кухтик С.Ю., Попова М.Ю., Танцурова К.С. Вестник Совета молодых учёных и специалистов Челябинской области, 2016
- Визуализация зрительного нерва в диагностике и мониторинге ретробульбарного неврита. Юрьева Т.Н., Бурлакова Е.В., Худоногов А.А., Аюева Е.К., Сухарчук О.В. Acta Biomedica Scientifica, 2011. с. 133-136
- Современный взгляд на проблему оптического неврита (систематический обзор). Кривошеева М.С., Иойлева Е.Э. Саратовский научно-медицинский журнал, 2020. с. 602-605
- Результаты лечения оптического неврита. Латыпова Э.А. Саратовский научно-медицинский журнал, 2018. с. 875-879
Статья опубликована: 15.02.2018 г. Последнее обновление: 28.09.2021 г. Читайте также Воспаление лимфоузлов
Воспаление лимфоузлов (лимфаденит) – их специфическое или неспецифическое воспалительное поражение. Развивается при попадании в лимфатическую систему различных микр…

Ожирение – один из главных факторов, увеличивающих риск преждевременной смерти, так как при этом высока вероятность развития целой группы заболеван…
Остеопороз – «коварное» заболевание
Остеопороз – это прогрессирующее заболевание скелета, характеризующееся снижением массы костей и нарушением структуры (микроархитектоники) костной …
Все лекции для врачей удобным спискомПоделиться:12 сентября 2021
Лекция для врачей “МРТ черепных нервов” Лекцию для врачей проводит к. м. н. Трофимова Т. Н.
На лекции рассмотрены следующие вопросы:
- Актуальность
- Поражение черепных нервов, является одной из актуальных проблем неврологии и нейрохирургии
- Проблема выбора тактики лечения пациентов с симптомами дисфункции черепных нервов (ЧН)
- Обширный спектр заболеваний, приводящих к дисфункции черепных нервов (ЧН)
- Отсутствие стандартизированного комплекса диагностических исследований
- Визуализация и определение изменений черепных нервов (ЧН) и прилежащих структур были возможны интраоперационно или при аутопсии
- MPT вносит существенный вклад в решение этой задачи:
- безопасность
- высокая тканевая контрастность и разрешающей способности
- возможность получения изображений в различных плоскостях
- Методология
- высокая напряженность магнитного поля (1,5 Т)
- наличие ИП – FIESTA и SPGR, 3 плоскости
- пакет опций для постпроцессинговой обработки изображений (MPR, MIP)
- Уровни поражения
- ядра
- цистерны ствола и основания
- костные каналы
- кавернозный синус или верхняя глазничная щель
MPT с контрастированием
- MPT с контрастным усилением является ценным для обнаружения и дифференцировки изменений черепных нервов
- Патологическое усиление MP-сигнала от структур нерва и окружающих тканей на МРТ может иногда быть первым в определении основной причины заболевания
- 3D-SPGR-ИП + “С”
- очаги демиелинизации
- мелкие невриномы, менингиомы
- Постконтрастная МРА – дифференциация вазоневральной компрессии
Стандартное исследование головного мозга
- Поражение III III IV V VI VII VIII IX XI XII черепных нервов
- Материалы и методы
- Комплексное клинико-лучевое обследование проведено 618 пациентам, из них 160 с невралгией тройничного нерва
- Клиническое обследование – невролог, нейрохирург, окулист, оториноларинголог, психиатр
- Инструментальное исследование
- Лучевая диагностика – краниография, КТ и КТА, МРТ и MPA, СКТ лицевого скелета
- Показания к МРТ
- Опухоли, кисты
- Демиелинизирующие процессы
- Воспалительные заболевания
- Цереброваскулярные заболевание
- Аномалии развития
- Показания к КТ
- Изучение костных каналов черепных нервов и их выходных отверстий
- СКТ- ангиография с визуализацией сосудов головного мозга и последующей объемной реконструкцией на фоне костей основания черепа
- Виртуальное планирование хирургического лечения
- Противопоказания для выполнения МРТ
- Методика лучевого исследования черепных нервов
- I этап – стандартное МРТ исследование головного мозга
- II этап – специализированный протокол для изучения структур цистернальной части черепных нервов (3D-FIESTA ИП и 3D-SPGR ИП, толщина среза 1,00 мм)
- III этап – МРТ и МРА с контрастированием
- IV этап – стандартная методика СКТ с последующей объемной 3-D реконструкцией (тонкие срезы -1,5 мм)
- V этап – КТА
- Изучение структур цистернальной части черепных нервов
- Реформатирование
- МР ангиография
- I – обонятельный нерв
- Эстезионейробластома
- Невринома обонятельного нерва
- Пациент, 60 лет, аносмия. МРТ. Менингиома площадки клиновидной кости и ольфакторной ямки
- Пациент, А., 52 г., аносмия МРТ. Невринома обонятельного нерва
- Зрительные нервы
- Астроцитома хиазмы
- Детский возраст (+/- нейрофиброматоз)
- Гетерогенное усиление
- Супраселлярная локализация
- +/- распространение на зрительные тракты
- Анапластическая астроцитома (нейрофиброматоз)
- Билатеральная глиома оптических путей
- Гамартоматозные поражения моста, ножек мозга, латеральных базальных ядер, зрительных бугров
- МТС по оболочкам (спустя 2 года)
- Рассеянный склероз
- III – глазодвигательный нерв. Блок срезов ориентирован по ходу цистернальной порции глазодвигательного нерва проекционно на ножки мозга (область межножковой цистерны)
- Изображение глазодвигательного нерва
- III – глазодвигательный нерв
- Нейроваскулярный конфликт
- Компрессия зоны входа правого блокового нерва (цистернальная порция) петлей верхней мозжечковой артерии
- Методика MPT тройничного нерва
- Блок срезов располагается в зоне входа корешка тройничного нерва в мост (по Т2-ВИ/Т1-ВИ в сагиттальной или Т2-ВИ в корональной плоскостях, ориентируясь на локализацию ствола тройничного нерва в боковых цистернах моста)
- Аксиальная плоскость
- Сагиттальная плоскость
- Корональная плоскость
- Гассеров узел
- V – тройничный нерв. Анатомо-топографические соотношения тройничного нерва и сосуда в норме
- V – тройничный нерв. Ростральный тип компрессии
- V – тройничный нерв. Латеральный тип компрессии
- Компрессия тройничного нерва основной артерией
- Тройничный нерв. ABM
- Тройничный нерв. Инфаркт продолговатого мозга (в месте расположения ядер V)
- Тройничный нерв. Кавернома
- Тройничный нерв. Рассеянный склероз
- Тройничный нерв. Менингит
- Тройничный нерв. Цитомегаловирусная инфекция
- Тройничный нерв. Саркоидоз
- Невринома тройничного нерва
- Наиболее часто ЧН У (полость Меккеля)
- Обычно хорошо очерчена
- Форма гантели с ЦП компонентом
- Обычно гиперинтенсивна на Т2-ВИ
- Одиночная/множественная (NF2)
- Одно/билатеральная локализация Т1-ВИ
- Меккелева полость
- Признак «подмигивающей» Меккелевой полости (один «глаз» закрыт): плотность/интенсивность не соответствует ликвору
- Патологические изменения дистальной части У ЧИ и иннервируемым им мышцам
- Острый процесс – гиперинтенсивность и +С мышцы
- Хронический – атрофия X и жировая дегенерация
- Невринома тройничного нерва
- Образование овальной формы, широким основанием прилежащее к твердой оболочке петрокливального региона, распространяющееся в задние отделы. Меккелевой полости, V нерв компремирован
- 3-D реконструкция выходных каналов I ветвей V ЧН
- Варианты расположения тригеминальных каналов и выходных отверстий
-
- Надглазничное отверстие(средняя треть глазницы – 83%)
- Одиночная надглазничная вырезка -60%
- Отверстие канала – 21% Множественные отверстия ипсилатеральной локализации – 17%
- Отсутствие надглазничного отверстия -1,5%
-
- Варианты расположения тригеминальных каналов и выходных отверстий
- Подглазничный канал (уровень скулочелюстного шва, лунка 5 зуба – 66%, длина – 10-15 мм)
- Два подглазничных отверстия -10%
- Форма – округлая, полуовальная, щелевидная
- Подглазничный канал (уровень скулочелюстного шва, лунка 5 зуба – 66%, длина – 10-15 мм)
- Варианты расположения тригеминальных каналов и выходных отверстии
- VI — отводящий нерв. Методика МРТ
- Блок срезов устанавливается в проекции нижней поверхности моста где корешки отводящего нерва располагаются в борозде между мостом и пирамидой
- Методика MPT VII и VIII
- Блок срезов устанавливается аксиально, каудальнее места расположения срезов при получении изображения тройничного нерва, ориентируясь на изображение внутреннего слухового прохода
- 1 – цистернальная часть лицевого нерва – 2,1 мм
- VIII — преддверно-улитковый нерв
- Преддверно-улитковый нерв (1) начинается от собственных ядер, расположенных в латеральной части ромбовидной ямки
- Показывается на нижней поверхности мозга кнаружи от оливы продолговатого мозга в виде двух корешков: вестибулярного (2) и улиткового (3)
- Поражение преддверно-улиткового нерва
- опухоли ММУ, сосудистые, демиелинизирующие или дегенеративные заболевания
- Поражение вестибулярного анализатора (внутреннего уха, вестибулярного нерва, ствола мозга):
- головокружение
- нистагм
- вестибулярная атаксия
- Поражение слухового анализатора:
- шум в ухе
- снижение слуха
- Анатомо-топографические соотношения ЗИМА и VII VIII ЧН в норме
- Компрессия лицевого нерва ПА
- Нейроваскулярный конфликт VII VIII ЧН
- Невринома
- Саркоидоз VII, карциноматоз VII, герпес VII
- Аплазия левого VIII
- Каудальная группа черепных нервов
- Блок срезов в аксиальной плоскости ориентирован параллельно преддверно-улитковым нервам, корональные срезы – вдоль оси продолговатого мозга
- IX языкоглоточный и X блуждающий нервы
- Компрессия языкоглоточного и блуждающего нервов ЗНМА
- Обширные патологические массы, компремирующие правые отделы ствола, распространяющиеся экстракраниально через яремное отверстие
- Компрессия IX нерва ЗНМА
- XI — добавочный нерв
- XII — подъязычный нерв
- Невринома каудальной группы нервов
Интернет-магазин медицинской литературы
Бесплатные лекции для врачей. Удобным списком
Порядка 40 млн слепых людей во всем мире нуждаются в технологиях, которые могут вернуть способность видеть. Однако до сих пор не существует доступного способа протезирования зрения
Мы привыкли ассоциировать зрение лишь с глазами. Однако помимо самих глазных яблок в процессе участвует зрительная кора головного мозга, которой мы фактически «видим», и нервные пути, которые соединяют глаза с мозгом. Практически на каждом этапе можно попытаться реализовать протезирование.
История создания зрительного протеза
Немецкий психолог Иоганн Пуркинье в 1823 году заинтересовался вопросами зрения и галлюцинаций, а также возможностью искусственной стимуляции зрительных образов. Принято считать, что именно он впервые описал зрительные вспышки — фосфены, которые он получил при проведении простого опыта c аккумулятором, пропуская через голову электрический ток и описывая свой визуальный опыт.
Спустя 130 лет, в 1956 году, австралийский ученый Дж. И. Тассикер запатентовал первый ретинальный имплант, который не давал какого-то полезного зрения, но показал, что можно искусственно вызывать зрительные сигналы.
Ретинальный имплант (имплант сетчатки) «вводит» визуальную информацию в сетчатку, электрически стимулируя выжившие нейроны сетчатки. Пока вызванные зрительные восприятия имели довольно низкое разрешение, но достаточное для распознавания простых объектов.
Но глазное протезирование долго тормозилось из-за технологических ограничений. Прошло очень много времени, прежде чем появились какие-то реальные разработки, которые смогли дать «полезное зрение», то есть зрение, которым человек мог бы воспользоваться. В 2019 году в мире насчитывалось около 50 активных проектов, фокусирующихся на протезировании зрения.
Первые ретинальные импланты
Пару лет назад на рынке было доступно три ретинальных импланта, которые прошли клинические испытания и были сертифицированы государственными регулирующими органами: европейским CE Mark и американским FDA.
- Second Sight Medical Products, США
- Pixium Vision, Франция
- Retina Implant AG, Германия
Так выглядели первые ретинальные импланты
Бионические импланты — это целая система внешних и внутренних устройств.
IRIS II (Pixium Vision) и Argus II (Second Sight) имели внешние устройства (очки с видеокамерой и блок обработки видеосигнала). Слепой человек смотрит при помощи камеры, с нее картинка направляется в процессор, где изображение обрабатывается и распадается на 60 пикселей (для системы Argus II). Затем сигнал направляется через трансмиттер на электродную решетку, вживленную на сетчатке, и электрическим током стимулируются оставшиеся живые клетки.
В немецком импланте Alfa АMS (Retina Implant) нет внешних устройств, и человек видит своим собственным глазом. Имплант на 1600 электродов вживляется под сетчатку. Свет через глаз попадает на светочувствительные элементы и происходит стимуляция током. Питается имплант от подкожного магнитного коннектора.
Субретинальный имплантат Alpha AMS компании Retina Implant AG
Все три ретинальных импланта больше не производятся, так как появилось новое поколение кортикальных протезов (для стимуляции коры головного мозга, а не сетчатки глаза). Однако хотя проектов по фундаментальным разработкам по улучшению ретинальных имплантов еще много, ни один из них не прошел клинические испытания:
- Улучшенный имплант DRY AMD PRIMA компании Pixium с увеличением количества электродов для стимуляции большего количества клеток сетчатки проходит клинические испытания. Для участия в программе испытаний еще ищут пять кандидатов;
- Retina Implant AG закрыли производство;
- Second Sight проводят клинические испытания своего кортикального импланта, но в марте 2020 года компания уволила 80% сотрудников из эксплуатационно-производственного подразделения.
Тренды ретинальных имплантов: основные фундаментальные технологии
Ретинальные нанотрубки
Группа ученых из Китая (Shanghai Public Health Clinical Center) в 2018 году провела эксперимент на мышах, в ходе которого вместо не функционирующих фоторецепторов сетчатки предложила использовать нанотрубки. Преимущество этого проекта — маленький размер нанотрубок. Каждая из них может стимулировать только несколько клеток сетчатки.
Биопиксели
Группа ученых из Оксфорда стремится сделать протез максимально приближенным к естественной сетчатке. Биопиксели в проекте выполняют функцию, схожую с настоящими клетками. Они имеют оболочку из липидного слоя, в который встроены фоточувствительные белки. На них воздействуют кванты света и как в настоящих клетках изменяется электрический потенциал, возникает электрический сигнал.
Перовскитная искусственная сетчатка
Все предыдущие фундаментальные разработки направлены на стимулирование всех слоев живых клеток. При помощи технологии перовскитной искусственной сетчатки китайские ученые пытаются предоставить возможность не только получать световые ощущения, но и различать цвет за счет моделирования сигнала таким образом, чтобы он воспринимался мозгом как имеющий определенную цветность.
Фотогальваническая пленка Polyretina
В Polyretina используется маленькая пленка, покрытая слоем химического вещества, которое имеет свойство поглощать свет и конвертировать его в электрический сигнал. Пленка размещена на сферическом основании, чтобы можно было удобно разместить ее на глазном дне.
Фотогальванический имплант Polyretina
Субретинальное введение полупроводникового полимера
Итальянские ученые предлагают технологию введения полупроводникового полимерного раствора под сетчатку, при помощи которого свет фиксируется и трансформируется в электрические сигналы.
Российский опыт ретинального протезирования
В России в 2017 году при поддержке фондов «Со-единение» и «Искусство, Наука и Спорт» было приобретено и установлено два ретинальных импланта Argus II американской компании Second Sight. Это единственные операции по восстановлению зрения, которые были проведены в России за все время. Каждая операция вместе с реабилитацией стоила порядка 10 млн руб, а сама система имплантации для одного пациента — порядка $140 тыс. Все прошло успешно, и два полностью слепых жителя Челябинска — Григорий (не видел 20 лет) и Антонина (не видела 10 лет) — получили предметное зрение. Предметное зрение означает, что человек может видеть очертания предметов — дверь, окно, тарелку — без деталей. Читать и использовать смартфон они не могут. Оба пациента имели диагноз «пигментный ретинит» (куриная слепота).
На момент 2019 года в мире установлено около 350 имплантов, произведенных компанией Second Sight. Около 50 тысяч россиян нуждаются в подобном протезе сетчатки.
В России опытом в протезировании зрения может похвастаться лишь один проект — АНО Лаборатория «Сенсор-Тех».
«Трендом в фундаментальных разработках бионических протезов является стремление сделать их максимально безопасными, приближенными к биологическим тканям людей и с максимально возможным разрешением. Но настоящую революцию вызвали кортикальные импланты, и смысл в ретинальных имплантах пропал, так как они ставятся только при пигментном ретините и возрастной макулярной дегенерации при отсутствии ряда противопоказаний. Кортикальные же импланты значительно расширяют горизонт показаний и позволяют восстанавливать полезное зрение даже людям, вовсе лишенным глаз», — рассказал Андрей Демчинский, к.м.н., руководитель медицинских проектов АНО Лаборатория «Сенсор-Тех».
Кортикальные системы имплантации
Кортикальные протезы — это подгруппа визуальных нейропротезов, способных вызывать зрительные восприятия у слепых людей посредством прямой электрической стимуляции затылочной коры мозга, которая отвечает за распознавание изображений. Этот подход может быть единственным доступным лечением слепоты, вызванной глаукомой, терминальной стадией пигментного ретинита, атрофией зрительного нерва, травмой сетчатки, зрительных нервов и т.п. За последние пять лет ученые решили задачу создания такого внутрикортикального визуального нейропротеза, с помощью которого можно было бы восстановить ограниченное, но полезное зрение.
В 1968 году Г.С. Бридли и В.С. Левин провели первую операцию по установке кортикальных имплантов. Первый имплант состоял из шапочки с коннекторами (устанавливали на череп под кожу) и отдельной дуги с электродами (устанавливали под череп), которые стимулировали кору головного мозга. Эксперимент был проведен на двух добровольцах для оценки возможности получения полезного зрения. Позднее импланты были извлечены. Технология кортикальных имплантов была заморожена по причине провоцирования приступов эпилепсии при стимуляции большего количества клеток мозга.
Первый кортикальный имплант
Кортикальный имплант Orion
Спустя 45 лет американский лидер разработки ретинальных имплантов Second Sight создал кортикальную протезную систему ORION. В конце 2017 года Second Sight получили разрешение от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) на проведение клинических испытаний. До апреля 2018 года было установлено шесть устройств. По результатам испытаний оказалось, что все пациенты ощущали зрительные стимулы, a у трех пациентов результаты были схожи с ретинальным имплантом Argus II и дали полезное предметное зрение. Клинические испытания будут проходить до июня 2023 года. Обязательным условием установки импланта является наличие у пациента зрительного опыта, то есть он может использоваться только для людей со сформированной зрительной корой, которые родились зрячими и потеряли зрение.
Система кортикальной имплантации Orion компании Second Sight
Кортикальный нейропротез CORTIVIS
Испанские ученые разработали кортикальный имплант под названием CORVITIS. Протез состоит из нескольких компонентов. Одна или две камеры обеспечивают получение изображения, которое затем обрабатывается биопроцессором, чтобы преобразовать визуальный образ в электрические сигналы. На втором этапе информация сводится в серию изображений и передается по радиочастотной связи на имплантированное устройство. Этот радиочастотный блок обеспечивает беспроводную передачу питания и данных во внутреннюю систему. Имплантированный электронный блок декодирует сигналы, определяет и контролирует форму напряжения и амплитуду формы волны, которая будет подаваться на соответствующие электроды. Клинические испытания на пяти пациентах завершатся в мае 2023 года.
Кортикальный имплант CORVITIS
Интракортикальный зрительный протез (WFMA)
Американские ученые разработали технологию многоканальной внутрикортикальной стимуляции с помощью беспроводных массивов металлических микроэлектродов и создали беспроводную плавающую микроэлектродную решетку (WFMA).
Система протеза состоит из группы миниатюрных беспроводных имплантируемых решеток-стимуляторов, которые могут передавать информацию об изображении, снятом на встроенную в очки видеокамеру, непосредственно в мозг человека. Каждая решетка получает питание и цифровые команды по беспроводной связи, так что никакие провода или разъемы не пересекают кожу головы. Посылая команды в WFMA, изображения с камеры передаются непосредственно в мозг, создавая грубое предметное визуальное восприятие изображения. Хотя восприятие не будет похоже на нормальное зрение, с его помощью человек может вести самостоятельную деятельность. Система ICVP получила одобрение FDA для проведения клинических испытаний.
Интракортикальный зрительный протез (WFMA)
Кортикальный протез NESTOR
Голландские ученые также разработали схожую технологию системы протезирования. Принцип функционирования протеза такой же, как в проектах выше. Камера отправляет сигнал на имплант, который состоит из тысяч электродов и смарт-чипа. С помощью процессора зрительное восприятие можно контролировать и регулировать.
«Хотя полное восстановление зрения пока кажется невозможным, кортикальные системы создают по-настоящему значимые визуальные восприятия, при помощи которых слепые люди могут распознавать, локализировать и брать предметы, а также ориентироваться в незнакомой среде. Результат — в существенном повышении уровня жизни слепых и слабовидящих. Такие вспомогательные устройства уже позволили тысячам глухих пациентов слышать звуки и приобретать языковые способности, и такая же надежда существует в области визуальной реабилитации», — обнадежил Андрей Демчинский.
Обновлено 14.08.2020Главная › Диагностика › Диагностика вызванных потенциалов › Наши преимущества: Ежегодно получают медицинскую помощь около 20 тысяч человек, из них более двух тысяч грудных детей. Учреждение полностью автоматизировано, ведется электронная карта пациента Более 60 высоко- квалифицированных врачей с большим клиническим опытом Медицинский центр с 1991 года профессионально занимается обучением врачей-неврологов –>
- Позвоните нам по номеру регистратуры.
- Консультант порекомендует вам специалиста.
- Запишитесь на прием в свободные для приема часы.
- Оплатите услугу по прейскуранту, используя систему оплаты на сайте по банковской карте, либо квитанцией через Сбербанк. Подробнее
- Приходите на прием в соответствии с назначенным временем консультации.
- При неоказании услуги медицинский центр делает 100% возврат средств.
Показания для ЭНМГ-исследования:
- болезни двигательных нейронов (спинальные мышечные атрофии, боковой амиотрофический склероз, миелопатии и др.)
- радикулопатии (вертеброгенные и невертеброгенные)
- плексопатии плечевого и пояснично-крестцового сплетений (посттравматические; постлучевые; компрессионные, в том числе синдром верхней апертуры грудной клетки; дизиммунные, в том числе невралгическая амиотрофия Персонейджа-Тернера и др.)
- полинейропатии (диабетические, токсические, дефицитарные, при хронических соматических заболеваниях; дизиммунные – синдром Гийена-Барре, хроническая воспалительная демиелинизирующая полинейропатия, парапротеинемические, васкулит-ассоциированные, наследственные и др.)
- мононейропатии, множественные мононейропатии (компрессионные, посттравматические, дизиммунные, мультифокальная моторная нейропатия)
- миастения и миастеноподобные заболевания, синдром Ламберта-Итона
- миопатии разного генеза, наследственные мышечные дистрофии, миотонии и др.
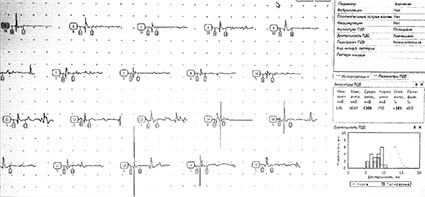
Как проходит обследование? При проведении ЭНМГ Вас попросят раздеться (частично или полностью до белья), сесть или лечь на кушетку. Небольшой участок кожи в месте исследования будет обработан спиртом. При ЭНМГ на мышцу наложат поверхностные электроды (липучки на клейкой основе или чашечки, фиксируемые на коже лейкопластырем), после чего стимулирующим электродом будут наноситься электрические стимулы на различные области руки или ноги в проекции хода нерва. Сила тока тем сильнее, чем глубже располагается нерв. иЭМГ проводится без использования электрического тока, на небольшую глубину в расслабленную мышцу вводится игольчатый электрод, специалист просит вас расслабиться или напрячь мышцу, 3-4 раза меняется положение игольчатого электрода в мышце.
В некоторых случаях оба метода (ЭНМГ и иЭМГ) используются одномоментно: например, при травмах нервов, при радикуло- и плексопатиях, в сложных диагностических случаях и др.
Какой метод ЭНМГ мне нужен? Выбор метода ЭНМГ, а также объем исследования определяет лечащий врач или специалист ЭНМГ, исходя из предполагаемого диагноза, указанного в направлении на обследование. Если ваш лечащий врач, рекомендующий ЭНМГ-исследование, заполнит данное направление, в этом случае можно рассчитывать на то, что проведенное обследование будет выполнено наиболее исчерпывающее, чётко под задачи, поставленные врачом перед нейрофизиологом. Обращаем ваше внимание, что ЭНМГ – это комплекс разных методик исследования с разной диагностической значимостью при том или ином уровне поражения периферического нейро-моторного аппарата. В зависимости от задач, поставленных лечащим врачом, врач-нейрофизиолог индивидуально подбирает необходимые методики обследования. Заполнение направления вашим врачом (образец направления) поможет правильно составить объем исследования, исключит выполнение ненужных проб, ускорит установление точного диагноза и избавит вас от повторных визитов на ЭНМГ.
- Направление на ЭНМГ
Как долго проводится ЭНМГ? Длительность обследования зависит от направительного диагноза и поставленных задач. В среднем исследование длится в течение 30 минут, но может в сложных случаях продолжаться и дольше.
ОСНОВНЫЕ ОГРАНИЧЕНИЯ ЭНМГ:
- не оцениваются тонкие чувствительные и вегетативные нервные волокна
- не все нервы и мышцы доступны для ЭНМГ-обследования, а при исследовании некоторых имеются методологические трудности
- при остром развитии заболевания ЭНМГ-изменения “запаздывают” за клиническими симптомами (в этой связи при острых нейропатиях любого генеза оптимально проводить исследование не ранее, чем через 2-3 недели от появление первых симптомов)
- имеются методологические трудности исследования при отеках, трофических нарушениях кожи, повышенной массе тела
ПРОТИВОПОКАЗАНИЙ К ПРОВЕДЕНИЮ ЭНМГ НЕТ. Исключением является нарушение целостности кожных покровов (травма, инфекция) в месте наложения электродов. Кроме того, ЭНМГ не может проводиться в случае, если на конечность, которую необходимо обследовать, наложена повязка, гипс или лонгета.
ПОДГОТОВКА К ИССЛЕДОВАНИЮ:
- перед исследованием можно все кушать и пить – ограничений нет, можно принимать назначенные вам препараты (исключением является прием антихолинэстеразных препаратов (прозерин, калимин) перед проведением декремент теста)
- накануне необходимо принять душ, соблюдать элементарные правила гигиены кожи
- не рекомендуется наносить на кожу крема или лосьоны
- необходимо держать руки и ноги в тепле, не переохлаждаться
ЧТО ВЗЯТЬ С СОБОЙ НА ИССЛЕДОВАНИЕ?
- направление от лечащего врача с обязательным указанием предварительного диагноза и цели исследования
- желательно иметь простынь или пеленку
Перед проведением исследования предупредите, пожалуйста, специалиста о следующих состояниях:
- Страдаете ли Вы эпилепсией, склонны ли Вы к синкопальным состояниям?
- Стоит ли у Вас водитель сердечного ритма?
- Являетесь ли Вы носителем ВИЧ-инфекции, сифилиса, гепатита и прочих инфекций?
- Нет ли у Вас обострения кожных заболеваний, повреждений кожи?
- Получаете ли Вы антикоагулянтную терапию – препараты, разжижающие кровь?
- Беременны ли Вы?
- Укажите были ли у Вас переломы конечностей, где именно?
В ФГБНУ НЦН на базе лаборатории клинической нейрофизиологии и центра заболеваний периферической нервной системы проводится весь комплекс электронейромиографических исследований любой сложности на оборудовании экспертного класса (миографы Dantec Keypoint, Нейрософт Нейро-МВП-4). Исследование проводят специалисты с большим опытом работы, что гарантирует Вам проведение обследования в полном объеме и грамотную интерпретацию данных. Нашим ЭНМГ-специалистам приходится сталкиваться с самыми сложными и редкими заболеваниями, высокий уровень подготовки позволяет решить поставленные задачи в большинстве случаев.
05.09.19